
��Ӧ����v�ͷ�Ӧ��Ũ�ȵĹ�ϵ����ʵ�鷽���ⶨ�ġ���ѧ��ӦH2+Cl2 2HCl�ķ�Ӧ����v�ɱ�ʾΪv��k��c��H2����m��c��Cl2����n��ʽ��kΪ������m��nֵ�����±�������ȷ����
2HCl�ķ�Ӧ����v�ɱ�ʾΪv��k��c��H2����m��c��Cl2����n��ʽ��kΪ������m��nֵ�����±�������ȷ����
|
c��H2��/��mol��L��1�� |
c��Cl2��/��mol��L��1�� |
v/��mol��L��1��s��1�� |
|
1.0 |
1.0 |
1.0 k |
|
2.0 |
1.0 |
2.0 k |
|
2.0 |
4.0 |
4.0 k |
�ɴ˿��Ƶã�m��nֵ��ȷ���ǣ�
A��m��1��n��1 B��m��1/2��n��1/2 C��m��1/2��n��1 D��m��1��n��1/2

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 3 |
| 2 |
| 1 |
| 3 |
| 2 |
| 3 |
| ���� | ��Ӧ��Ͷ����� | ��Ӧ���ת���� | CH3OH��Ũ�� | �����仯 ��Q1��Q2��Q3������0�� |
| �� | 1mol CO��2mol H2 | a1 | c1 | �ų�Q1kJ���� |
| �� | 1mol CH3OH | a2 | c2 | ����Q2kJ���� |
| �� | 2mol CO��4mol H2 | a3 | c3 | �ų�Q3kJ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��
CO(g)+2H2(g)![]() CH3OH(g)��
CH3OH(g)��

��1���÷�Ӧ��ƽ�ⳣ������ʽΪ��K=
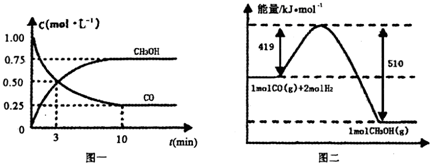
��2��ͼ1�Ƿ�ӦʱCO��CH3OH(g)��Ũ����ʱ��ı仯������ӷ�Ӧ��ʼ��ƽ�⣬��COŨ�ȱ仯��ʾ��ƽ����Ӧ����v(CO��= ��
��3�����˵Ĵ����� ��ѡ����ţ���
a.�ı䷴Ӧ����ЧӦ b.���������ܺ� c.�ӿ췴Ӧ����
d.��߷�Ӧ���ת����
��4����2 L�ܱ������з�����Ӧ CO(g)+2H2(g) ![]() CH3OH(g) ��T��ʱ������2mol CH3OH����Ӧ��ƽ�������CO 1 mol����ʱ��������ͬʱ����2 mol��CH3OH��4mol��H2������壨�����¶Ȳ��䣩����ƽ�⽫ ���������Ӧ���������淴Ӧ���������ƶ����ﵽ��ƽ���ƽ�ⳣ��K��ֵΪ
CH3OH(g) ��T��ʱ������2mol CH3OH����Ӧ��ƽ�������CO 1 mol����ʱ��������ͬʱ����2 mol��CH3OH��4mol��H2������壨�����¶Ȳ��䣩����ƽ�⽫ ���������Ӧ���������淴Ӧ���������ƶ����ﵽ��ƽ���ƽ�ⳣ��K��ֵΪ
��5�����������£����д�ʩ����ʹn (CH3OH)/n (CO)������� ��ѡ����ţ���
a. �����¶� b. ʹ�ô��� c.�ٳ���2mol H2 d.�ٳ���1mol CO
��6���״�������������ȼ�ϵ�أ��õ���ö�Ķ��Ե缫����Ũ����������Һ��д���õ�صĸ�����Ӧʽ___________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��
CO(g)+2H2(g)![]() CH3OH(g)��
CH3OH(g)��
��1���÷�Ӧ��ƽ�ⳣ������ʽΪ��K=
��2��ͼ1�Ƿ�ӦʱCO��CH3OH(g)��Ũ����ʱ��ı仯������ӷ�Ӧ��ʼ��ƽ�⣬��COŨ�ȱ仯��ʾ��ƽ����Ӧ����v(CO��= ��
��3�����˵Ĵ����� ��ѡ����ţ���
a.�ı䷴Ӧ����ЧӦ b.���������ܺ� c.�ӿ췴Ӧ����
d.��߷�Ӧ���ת����
��4����2 L�ܱ������з�����ӦCO(g)+2H2(g) ![]() CH3OH(g)��T��ʱ������2mol CH3OH����Ӧ��ƽ�������CO 1 mol����ʱ��������ͬʱ����2 mol��CH3OH��4mol��H2������壨�����¶Ȳ��䣩����ƽ�⽫ ���������Ӧ���������淴Ӧ���������ƶ����ﵽ��ƽ���ƽ�ⳣ��K��ֵΪ
CH3OH(g)��T��ʱ������2mol CH3OH����Ӧ��ƽ�������CO 1 mol����ʱ��������ͬʱ����2 mol��CH3OH��4mol��H2������壨�����¶Ȳ��䣩����ƽ�⽫ ���������Ӧ���������淴Ӧ���������ƶ����ﵽ��ƽ���ƽ�ⳣ��K��ֵΪ
��5�����������£����д�ʩ����ʹn (CH3OH)/n(CO)������� ��ѡ����ţ���
a. �����¶� b. ʹ�ô��� c.�ٳ���2mol H2 d.�ٳ���1mol CO
��6���״�������������ȼ�ϵ�أ��õ���ö�Ķ��Ե缫����Ũ����������Һ��д���õ�صĸ�����Ӧʽ___________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ��ӱ�ʡʯ��ׯ�и��������⡢ѹ���⻯ѧ�Ծ��������棩 ���ͣ������
.(13��)�ҹ��Ǹ��������,��������Ϊ�����һ,��¯��������Ϊ�ձ����������.
I.��֪��2CO(g)+ O2(g)��2CO2(g),��H��-566 kJ��mol-1
2Fe(s)+
 O2(g)��Fe2O3(s),��H��-825.5 kJ��mol-1
O2(g)��Fe2O3(s),��H��-825.5 kJ��mol-1
��Ӧ��Fe2O3(s)+
3CO(g) 2Fe(s)+ 3CO2(g),��H��______ kJ��mol-1.
2Fe(s)+ 3CO2(g),��H��______ kJ��mol-1.
��.��Ӧ 1/3Fe2O3(s)+
CO(g) 2/3Fe(s)+ CO2(g)��1000���ƽ�ⳣ������4.��һ���ݻ�Ϊ10L���ܱ�������,1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol,��Ӧ����l0min��ﵽƽ��.
2/3Fe(s)+ CO2(g)��1000���ƽ�ⳣ������4.��һ���ݻ�Ϊ10L���ܱ�������,1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol,��Ӧ����l0min��ﵽƽ��.
(1)CO��ƽ��ת����=____________.
(2)�����CO��ƽ��ת����,�ٽ�Fe2O3��ת��,�ɲ�ȡ�Ĵ�ʩ��________.
a����߷�Ӧ�¶� b������Ӧ��ϵ��ѹǿ
c��ѡȡ���ʵĴ��� d����ʱ���ջ��Ƴ�����CO2
e�������ʯ,ʹ����ƽ���������ֽӴ�
��.��¯���������ķ����е�CO�ɽ��л���,ʹ����һ�������º�H2��Ӧ�Ʊ��״�:
CO(g)+
2H2(g) CH3OH(g).�����ͼʾ�ش���������:
CH3OH(g).�����ͼʾ�ش���������:

(1)�ӷ�Ӧ��ʼ��ƽ��,��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)=________.
(2)�����¶Ⱥ�������ͬ�������ܱ�������,����ͬ��ʽͶ�뷴Ӧ��,��÷�Ӧ�ﵽƽ�ⅼ���й��������±�:
|
���� |
��Ӧ��Ͷ����� |
��Ӧ��� ת���� |
CH3OH��Ũ�� |
�����仯 (Q1��Q2��Q3������0) |
|
�� |
1mol CO��2mol H2 |
��1 |
c1 |
�ų�Q1 kJ���� |
|
�� |
1mol CH3OH |
��2 |
c2 |
����Q2 kJ���� |
|
�� |
2mol CO��4mol H2 |
��3 |
c3 |
�ų�Q3 kJ���� |
�����й�ϵ��ȷ����________.
A c1=c2 B.2Q1=Q3 C. 2��1=��2 D. ��1+��2=1
E. �÷�Ӧ������1mol CH3OH����ų�(Q1+Q2)kJ����
(3)����һ����ɱ���ܱ������г���l mol CO��2mol H2��1mol CH3OH,�ﵽƽ�ⅼ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6��,��÷�Ӧ��________(����������桱)��Ӧ�����ƶ�.
(4)�״�������������ȼ�ϵ��,�õ���ö�Ķ��Ե缫����Ũ����������Һ,д���õ�صĸ�����Ӧʽ___ ____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com