
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 | K+、Na+、Al3+、Cu2+ |
| 阴离子 | OH-、HCO3-、NO3-、SO42- |
(1) KNO3 (2分) ; KAl(SO4)2(带结晶水也同样给分)(2分)
(2)Al3++4OH-=AlO2-+2H2O(2分)
(3)Na2CO3 (2分)
(4) HCO3-+Ca2++OH-=CaCO3↓+H2O(或2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O)(2分)
(5)Al3++3H2O=Al(OH)3(胶体)+3H+ (2分) Al(OH)3(胶体)具有很强的吸附能
力,它能凝聚水中的悬浮物并使之沉降,从而达到净水的目的。(2分)
解析试题分析:①将它们溶于水后,D为蓝色溶液,说明D中含有离子Cu2+;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解,由以上离子可以看出,应为Al3+与OH-的反应,则E中含有OH-,C中含有Al3+;③进行焰色反应, B、C为紫色(透过蓝色钴玻璃),说明B、C中含有K+;④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,则A含有HCO3-,焰色反应不呈紫色,A应为NaHCO3,C、D中产生白色沉淀该沉淀为BaSO4,说明C、D中含有SO42-;所以C为KAl(SO4)2,D为CuSO4,E焰色反应不呈紫色,只能为NaOH,⑤将B、D两溶液混合,D为CuSO4,未见沉淀或气体生成,说明二者没有发生任何反应,则B为KNO3,则
(1)B、C的化学式分别为KNO3,KAl(SO4)2,(2)铝离子与过量氢氧化钠生成偏铝酸根。
(3)将含1mol A的溶液与含1mol E的溶液反应,反应的化学方程式为NaHCO3+NaOH═Na2CO3+H2O,溶液反应后蒸干,得到的化合物为Na2CO3,故答案为:Na2CO3;
(4)在NaHCO3溶液中加少入量澄清石灰水,其离子方程式为2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+H2O,
(5)Al2(SO4)2常作净水剂,原因是Al3+离子水解生成具有较强吸附性的Al(OH)3胶体,反应的离子方程式为Al3++3H2O  Al(OH)3+3H+,
Al(OH)3+3H+,
考点:考查元素化合物知识、离子反应、盐类水解等知识。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:填空题
已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:NH4+、Ba2+、Na+、H+、SO42-、NO3-、OH-、SO32-。将这四种溶液分别标记为A、B、C、D,进行如下实验。
①在A或D中滴入C,均有沉淀生成;
②D和B反应生成的气体能被A吸收;
③A和D反应生成的气体能被B吸收,也可使溴水褪色。
试回答下列问题:
(1)D的化学式是________,判断理由是___________________________________________。
(2)写出其余几种物质的化学式:A________,B________,C________。
(3)写出实验②中有关反应的离子方程式_______________________________。
(4)写出③中生成的气体与溴水反应的离子方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某混合溶液中可能含有的离子如下表所示:
| 可能大量含有的阳离子 | H+、Ag+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32—、AlO2— |
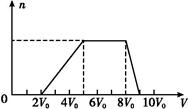
| Cl2的体积(标准状况) | 11.2 L | 22.4 L | 28.0 L |
| n(Cl-) | 2.5 mol | 3.5 mol | 4.0 mol |
| n(Br-) | 3.0 mol | 2.5 mol | 2.0 mol |
| n(I-) | x mol | 0 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某厂废水中含5.00×10-3 mol·L-1的Cr2O,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4(Fe的化合价依次为+3、+2),设计了如下实验流程: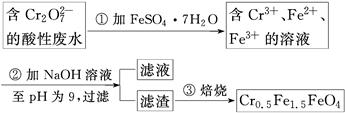
(1)第①步反应的离子方程式是________________________________________________。
(2)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有__________。
(3)欲使1 L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4。理论上需要加入________g FeSO4·7H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
亚氯酸钠(NaClO2)常用于水的消毒和砂糖、油脂的漂白与杀菌。以下是用过氧化氢法生产亚氯酸钠的工艺流程图: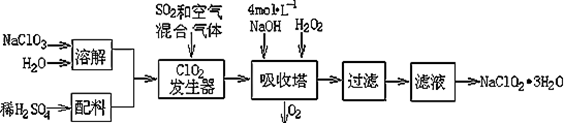
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O ;
②Ksp(FeS)=6.3×10-18 ; Ksp(CuS)=6.3×10-36 ;Ksp(PbS)=2.4×10-28
(1)吸收塔内发生反应的离子方程式为 。该工艺流程中的NaClO3、ClO2、NaClO2都是强氧化剂,它们都能和浓盐酸反应制取Cl2。若用二氧化氯和浓盐酸制取Cl2,当生成5 mol Cl2时,通过还原反应制得氯气的质量为 g。
(2)从滤液中得到NaClO2·3H2O晶体的所需操作依次是 (填写序号)。
a蒸馏;b灼烧;c过滤;d冷却结晶;e蒸发
(3)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2。
下表是 25℃时HClO2及几种常见弱酸的电离平衡常数:
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka/mol?L-1 | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10?8 K2=1.1×10?12 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铜单质及其化合物是应用极其广泛的物质。
(1)铜是氢后金属,不能与盐酸发生置换反应,但将单质铜置于浓氢碘酸中,会有可燃性气体及白色沉淀生成,又知氧化性:Cu2+>I2,则铜与氢碘酸反应的化学方程式为____________________________________________________。
(2)已知Cu2O能溶于醋酸溶液或盐酸中,同时得到蓝色溶液和红色固体,则Cu2O与稀硫酸反应的离子方程式为____________________________________;
Cu2O与稀硝酸反应的离子方程式为_____________________________;
只用稀硫酸来确定某红色固体是 Cu2O与Cu组成的混合物的方法:称取m g该红色固体置于足量稀硫酸中,充分反应后过滤,然后___________________。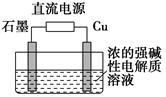
(3)Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解装置如图所示,电解总反应:2Cu+H2O电解,Cu2O+H2↑,则石墨应与电源的________极相连,铜电极上的电极反应式为________;电解过程中,阴极区周围溶液pH________(填“变大”、“变小”或“不变”)。
(4)现向Cu、Cu2O、CuO组成的混合物中加入1 L 0.6 mol/L HNO3恰好使混合物溶解,同时收集到2 240 mL NO(标准状况)。若将上述混合物用足量的氢气还原,所得固体的质量为________;若混合物中含有0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗硫酸的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)含氯消毒剂可防甲型H1N1流感。二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式_____________________________________________________________________________。
(2)某无色溶液只含有下列8种离子中的某几种:Na+、H+、Mg2+、Ag+、Cl-、OH-、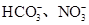 。已知该溶液可与Al2O3反应,则:
。已知该溶液可与Al2O3反应,则:
①该溶液与Al2O3反应后有Al3+生成,则原溶液中一定含有_______,一定不会含有大量的_______。
②该溶液与Al2O3反应后有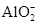 生成,则原溶液中一定含有_______,可能含有大量的_______。
生成,则原溶液中一定含有_______,可能含有大量的_______。
③写出该溶液与Al2O3反应生成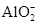 的离子方程式____________________________。
的离子方程式____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。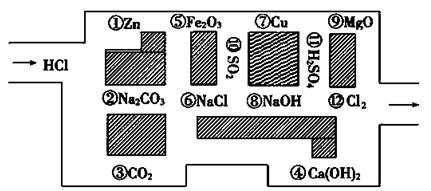
请根据要求在下列横线上填上合适的序号
(1)在迷宫中不能与稀盐酸反应的物质:属于电解质的是_______________,属于非电解质的是______________。
(2)在迷宫中的物质,能与稀盐酸发生氧化还原反应的是
(3)请你帮助它走出迷宫HCl—?—___—____—____—___—
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有下列物质:①氢氧化钠固体 ②铜丝 ③盐酸 ④熔融氯化钠 ⑤二氧化碳气体 ⑥氨水 ⑦蔗糖晶体。请用序号填空:
(1)上述状态下可导电的是________。 (2)属于电解质的是________。
(3)属于非电解质的是________。 (4)上述状态下的电解质不能导电的是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com