
【题目】某白色粉末A在农业上用作杀菌剂,进行下列实验:
①:白色粉末A溶解在水中,得到蓝色溶液,分成等量的两份
②:在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液;在此蓝色溶液中滴加酸化的AgNO3溶液又得到白色沉淀和蓝色溶液;
③:在①中的另一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硫酸钾溶液。
根据实验现象推断:
(1)A______________ B_______________ C_______________(填化学式)
(2)反应③中的离子方程式为__________________________________________________
【答案】CuSO4 BaCl2 KOH Cu![]() +2 OH—= Cu(OH) 2↓
+2 OH—= Cu(OH) 2↓
【解析】
①:白色粉末溶解在水中,得到蓝色溶液,说明此溶液中含有铜离子,验证了白色粉末为铜盐;
③:在①中的一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硫酸钾溶液,根据复分解反应规律可知,C溶液为KOH,铜盐为CuSO4;
②:在①中的另一份蓝色溶液(CuSO4)中加入适量的盐溶液B,恰好生成白色沉淀,过滤,蓝色滤液中含有铜离子;在此蓝色溶液中滴加酸化的AgNO3溶液又得到白色沉淀氯化银和蓝色溶液硝酸铜;从以上实验中可以确定白色沉淀和盐B各为硫酸钡和氯化钡; 据以上分析解答。
(1)①:白色粉末溶解在水中,得到蓝色溶液,溶液为蓝色,说明含有铜离子,白色粉末为铜盐;
③:在①中的一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硫酸钾溶液,根据复分解反应规律可知,C溶液为KOH,铜盐为CuSO4;
②:在①中的另一份蓝色溶液(CuSO4)中加入适量的盐溶液B,恰好生成白色沉淀,过滤,蓝色滤液中含有铜离子;在此蓝色溶液中滴加酸化的AgNO3溶液又得到白色沉淀氯化银和蓝色硝酸铜溶液;从以上实验现象中可知,白色沉淀为硫酸钡,盐B为BaCl2;
结合以上分析可知:A为CuSO4;B为BaCl2;C为KOH;
因此,本题正确答案是: CuSO4,BaCl2,KOH。
(2)硫酸铜溶液和氢氧化钾溶液反应生成氢氧化铜蓝色沉淀和硫酸钠溶液,离子方程式为:Cu2++2OH-=Cu(OH) 2↓;
综上所述,本题答案是:Cu2++2OH-=Cu(OH) 2↓。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用如图装置进行铁与水蒸气反应的实验,并检验产物的性质,请回答下列问题:
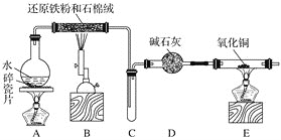
(1)A装置的作用是____________,烧瓶底部放碎瓷片的作用是_________________________。
(2)装置B中发生反应的化学方程式是____________________________________,该反应中氧化剂是__________,氧化产物是__________________。
(3)D的作用是__________________________________。
(4)E中的实验现象是____________________________。
(5)A、B两个装置中应先点燃________________处的酒精(喷)灯,点燃E处酒精灯之前应进行的操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关各实验的叙述中正确的是
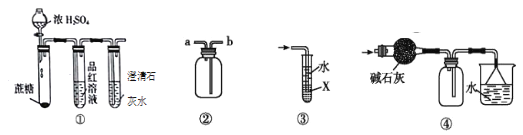
A. ①澄清石灰水变浑浊,证明蔗糖与浓硫酸反应生成了CO2
B. ②进行H2、NH3、CO2、Cl2、NO、NO2等气体的收集
C. ③当X选用苯时可进行NH3或HCl的吸收,并防止倒吸
D. ④可用于NH3的干燥,收集并吸收多余NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组在实验室制取 Na2O2。查阅资料可知:钠与空气在 453473K 之间可生成 Na2O,迅速提高温度到 573673K 之间可生成 Na2O2,若温度提高到 733873K 之间 Na2O2 可分解。
(1)甲组设计制取 Na2O2 装置如图1。
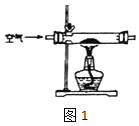
①使用该装置制取的 Na2O2 中可能含有的杂质为_____。.
A.NaCl B.Na2CO3 C.Na2O D.NaOH E.NaHCO3
②该小组为测定制得的 Na2O2 样品的纯度,设计可能用到的装置如图 2:烧瓶中发生的主要反应的化学方程式是_________。测定装置的接口从 左至右正确的连接顺序是_____。
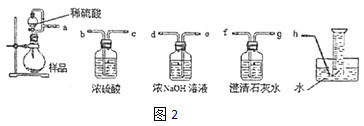
(2)乙组从反应历程上分析该测定反应存在中间产物,从而导致测定结果_____ (填“偏大”或“偏 小”)。为证明其分析的正确性,设计实验方案如下:
实验方案 | 产生的现象 |
Ⅰ.取烧瓶中的反应液加入少量 MnO2 粉末 | 有大量气泡逸出 |
Ⅱ.向 NaOH 稀溶液中加入 23 滴酚酞试液,然后加入少量的反应液 | 溶液先变红后褪色开始无明显现象。 |
Ⅲ.向反应液中加入 23 滴酚酞试液,充分振荡,然后逐滴加入 过量的 NaOH 稀溶液 | 加 NaOH 溶液先 变红后褪色 |
在上述实验中,能够证明乙组分析正确的最佳方案是_________ (填实验序号)。_______________组实验得不出结论,原因是_____。
(3)丙组根据上述提供的有关信息,设计一个方案可准确的测定样品的纯度。请简述实验操作和需 要测定的有关数据__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)金晶体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶角各有一个金原子,各个面的中心有一个金原子。金晶体每个晶胞中含有________个金原子。
(2)金和铜可以形成多种金属化合物,其中一种的晶体结构如下图所示(为面心立方结构)。该金属化合物的化学式________。
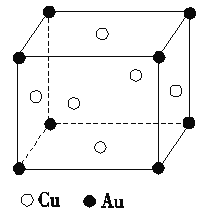
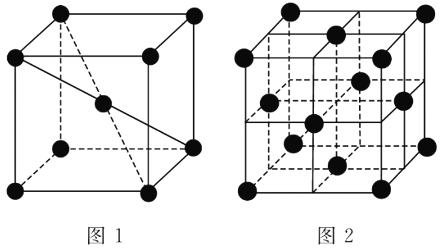
(3)1183 K以下纯铁晶体的基本结构单元如图1所示,1 183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的铁原子等距离且最近的铁原子数为________个;在1 183 K以上的纯铁晶体中,与铁原子等距离且最近的铁原子数为________。
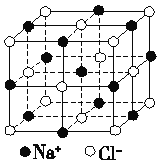
(4)如图为NaCl晶体结构图,图中直线交点处为NaCl晶体中Na+与Cl-所处的位置(不考虑体积的大小)。从晶胞中可以看出Na+周围与它最近时且距离相等的Na+共有________个。
(5)某离子晶体晶胞结构如图所示,X位于立方体的顶点,Y位于立方体中心。试分析:
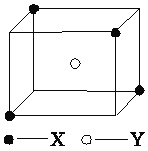
①晶体中每个Y同时吸引着________个X,每个X同时吸引着________个Y。
②晶体中在每个X周围与它最接近且距离相等的X共有________个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B. 在常温常压下,11.2L Cl2含有的分子数为0.5NA
C. 25℃,1.01×105Pa,64gSO2中含有的原子数为3NA
D. 标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中少量杂质所需除杂试剂及方法不正确的是( )
物质(杂质) | 除杂试剂 | 除杂方法 | |
A | 乙醇(水) | CaO | 蒸馏 |
B | 淀粉溶液(NaCl) | ——— | 渗析 |
C | CO2(HCl) | NaOH溶液 | 洗气 |
D | NaCl溶液(I2) | CCl4 | 萃取分液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同。
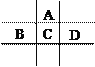
回答下列问题:
(1)A与E形成的化合物的化学式是 __________________。
(2)B的最高价氧化物化学式为____________,C的元素名称为 ___________________ 。
(3)D的单质与水反应的方程式为____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水CoCl2,故常在实验室中用作吸湿剂和空气湿度指示剂。
CoCl2+xH2O![]() CoCl2·xH2O
CoCl2·xH2O
深蓝色 粉红色
现有65 g无水CoCl2,吸水后变成CoCl2·xH2O 119 g。
(1)水合物中x=________。
(2)若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界占有Cl-的个数比为1∶1,则其化学式可表示为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com