
| A. | 盐酸 | B. | 氢氧化钠 | C. | 无水乙醇 | D. | 石灰水 |
分析 质量为a克的铜丝在酒精灯上加热灼烧后,生成CuO,插入到溶液中,放置片刻,铜丝质量不变,则CuO被还原为Cu,以此来解答.
解答 解:A.因铜片在酒精灯上加热后生成CuO,质量增加,将它投入盐酸中,发生反应:CuO+2HCl═CuCl2+H2O,Cu2+进入溶液,铜片的质量会减小,故A错误;
B.因铜片在酒精灯上加热后生成CuO,质量增加,将它投入NaOH中,不反应,铜片质量增加,故B错误;
C.因铜片在酒精灯上加热后生成CuO,质量增加,将它投入无水乙醇中,发生反应:CH3CH2OH+CuO→CH3CHO+H2O+Cu,又恢复为铜,铜片的质量不变,故C正确;
D.因铜片在酒精灯上加热后生成CuO,质量增加,将它投入石灰水中,不反应,铜片的质量会增加,故D错误;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握物质的性质、氧化还原反应及乙醇的催化氧化为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称量时,将NaOH固体放在右盘内的纸上,称得质量为10.2g | |
| B. | 用25mL碱式滴定管量取高锰酸钾溶液,体积为16.60mL | |
| C. | 用干燥的广泛pH试纸测稀盐酸的pH=3.2 | |
| D. | 用10mL量筒量取NaCl溶液,体积为9.2mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
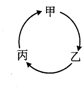 下表所列各组物质中,物质之间不能通过一步反应实现如图所示转化的是
下表所列各组物质中,物质之间不能通过一步反应实现如图所示转化的是| 选项、物质 | 甲 | 乙 | 丙 |
| A | SO2 | SO3 | H2SO4 |
| B | NH4Cl | NH3 | NO |
| C | Na | NaOH | NaCl |
| D | Al2O3 | AlCl3 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
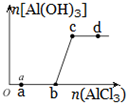 向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系示意如图所示.则的下列说法不正确的是( )
向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系示意如图所示.则的下列说法不正确的是( )| A. | a点对应的溶液中加入MgCl2无明显现象 | |
| B. | b点对应的溶液是NaAlO2溶液 | |
| C. | c点对应的溶液中c(Na+)=c(Cl-) | |
| D. | d点对应的溶液呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴极:4H2O+2O2-8e-═8OH- | B. | 正极:4H2O+2O2+8e-═8OH- | ||
| C. | 阴极:4OH-+4e-═2H2O+O2↑ | D. | 正极:4OH--4e-═2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
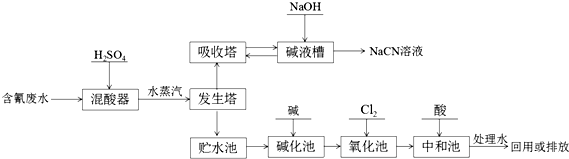
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
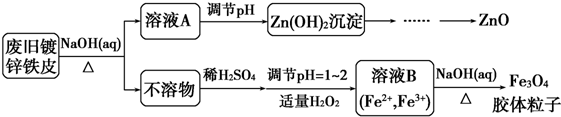
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
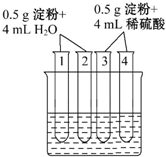 保持营养平衡,合理使用药物是保证身心健康、提高生活质量的有效手段.
保持营养平衡,合理使用药物是保证身心健康、提高生活质量的有效手段.| 编号 | 操作 | 现象 |
| 1 | 加入碘水 | 溶液变成蓝色 |
| 2 | 加入银氨溶液,水浴加热 | 未出现银镜 |
| 3 | 加入碘水 | 溶液变成蓝色 |
| 4 | 加入银氨溶液,水浴加热 | 未出现银镜 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com