
 ��
�� ��
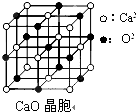
������ Ԫ�ص�ԭ�Ӻ���ֻ��1�����ӣ���AΪHԪ�أ�BԪ�ص�ԭ�Ӱ뾶����������������С�ģ�B������������Ӧˮ����Ļ�ѧʽΪHBO3����B������ϼ�Ϊ+5�ۣ�λ�����ڱ��ڢ�A�壬ӦΪNԪ�أ�CԪ��ԭ�ӵ������������ȴ�����4������ԭ�Ӻ�������Ų�Ϊ2��6��ӦΪOԪ�أ�C����������D�������Ӿ�����ͬ�ĵ����Ų�����Ԫ�ؿ��γɻ�����D2C����D�Ļ��ϼ�Ϊ+1�ۣ�ӦΪNaԪ�أ�C��E���壬��EΪSԪ�أ�����ԭ�ӵ���ɡ����ʽ�������ɵĵݱ���ɽ����⣮
��� �⣺�����Ϸ�����֪AΪHԪ�أ�BΪNԪ�أ�CΪOԪ�أ�DΪNaԪ�أ�EΪSԪ�أ���
��1��BΪNԪ�أ�B��ԭ�ӽṹʾ��ͼΪ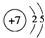 ��
��
�ʴ�Ϊ��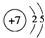 ��
��
��2��EΪSԪ�أ����Ϊ+6������������Ӧˮ����ΪH2SO4��
�ʴ�Ϊ��H2SO4��
��3��ͬ������ԭ����������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӱ뾶��Na��S��O��
�ʴ�Ϊ��Na��S��O��
��4��H��O����Ԫ���γɵ�ԭ�Ӹ���֮��Ϊ1��1�Ļ�����ΪH2O2��������Oԭ����Hԭ��֮���γ�1�Թ��õ��Ӷԡ�Oԭ��֮���γ�1�Թ��õ��Ӷԣ������ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��5�����������ᷴӦ��������泥���Ӧ���ӷ���ʽΪ��NH3+H+=NH4+��
�ʴ�Ϊ��NH3+H+=NH4+��
���� ���⿼��λ�ýṹ���ʹ�ϵӦ�ã���Ŀ�Ѷ��еȣ�ע����ȷ�ƶ�Ԫ�ص�����Ϊ������Ĺؼ�����Ҫѧ��ȫ�����ջ���֪ʶ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
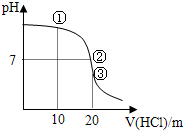
| A�� | ����Һ��c��Cl-����c��NH4+����c��OH-����c��H+�� | |
| B�� | ����Һ��c��NH4+��=c��Cl-��=c��OH-��=c��H��+ | |
| C�� | ����Һ�����е�����Ϊ5�� | |
| D�� | �ζ������п��ܳ��֣�c��NH4+����c��OH-����c��Cl-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
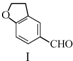 $\stackrel{CH_{2}��COOH��_{2}}{��}$
$\stackrel{CH_{2}��COOH��_{2}}{��}$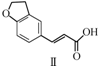 $��_{H_{2}}^{Pd-C}$
$��_{H_{2}}^{Pd-C}$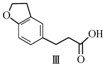
| A�� | ��������ˮ���ֻ������ͻ������ | |
| B�� | ������������NaHCO3��Һ������Ӧ | |
| C�� | 1 mol��������������3 mol H2�����ӳɷ�Ӧ | |
| D�� | �뻯�����Ϊͬ���칹�壬�ҷ����к���2��ȩ���ķ����廯������10�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʹ�õ�ʯ�͡�ú�ȴ�ͳ��Դ���������ܡ����ܵ�����Դ����������Щ��Դ������̫����ת���� | |
| B�� | ��������һ�����ܵ������ﱡĤ���м�ǿ�Ŀ���ʴ������������������������������ԡ�������ʳƷ�� | |
| C�� | �������ò�ľ�������ɻ�����ũҵ���ø������ֽ��֣���ҵ�����������δ���Ƥ��ȣ�����̵Ĺ�ͬ�㶼�������˵����ʱ��Ե����� | |
| D�� | �������������Ρ��������ȵȺ��Ȼ����ﶼ����ǿ�����ԣ�������ɱ���������Ȼ��ء������Ҳ�Ǻ��Ȼ������Ҳ������ɱ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 [���ʽṹ������]���������з�Ӧ�ϳ������谷��
[���ʽṹ������]���������з�Ӧ�ϳ������谷��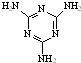 ���׳ơ����������������������谷���������ᣨ
���׳ơ����������������������谷���������ᣨ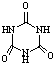 �������������������谷�����֮��ͨ�����Ӽ������ϣ������������γɽ�ʯ��
�������������������谷�����֮��ͨ�����Ӽ������ϣ������������γɽ�ʯ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���������ʱ�����ɵ��������������ӵ����� | |
| B�� | ���������ʱ�����ɵ������������������ӵ��Ǽ� | |
| C�� | ���������ʱ�����ɽ��������Ӻ�������ӵ����� | |
| D�� | NH4Cl���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com