
【题目】可逆反应A(g)+3B(g) ![]() 2C(g)+D(g) 在四种不同情况下的反应速率如下,其中反应进行得最快的是
2C(g)+D(g) 在四种不同情况下的反应速率如下,其中反应进行得最快的是
A.VA=0.15mol(Lmin)﹣1 B.VB=0.6 mol(Lmin)﹣1
C.VC=0.4 mol(Lmin)﹣1 D.VD=0.01 mol(Ls)﹣1
科目:高中化学 来源: 题型:
【题目】镁的化合物在化工生产和药物合成上有重要用途。某兴趣小组以一种工业废渣(主要成分为MgCO3、MgSiO3和少量Fe的氧化物)为原料制备MgCO3·3H2O。实验过程如下:

(1)废渣的成分为_________(填化学式),过滤装置在使用一段时间后需用NaOH溶液清洗,用化学方程式表示其清洗原理_____________________。
(2)加入H2O2的目的是__________________,一段时间后,溶液中有气泡出现并放热,则产生气泡的原因是____________。
(3)萃取分液中要用到分液漏斗,分液漏斗在使用前须洗干净并________________。萃取分液的目的是____________。(填序号)
A、除去水溶液中的铁离子
B、增加镁离子在水中的溶解性
C、富集铁元素,可以回收利用
(4)萃取后得到的水溶液制备MgCO3·3H2O的实验操作:边搅拌边向溶液中滴加Na2CO3溶液至有大量沉淀生成,静置,________,确定沉淀完全后,过滤、____________,得到MgCO3·3H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷和红磷均能在空气中燃烧,且燃烧产物相同,但二者的燃烧热不同,通过实验可测得这两个反应的反应热。
①![]() P4(s,白磷)+
P4(s,白磷)+![]() O2(g)=
O2(g)=![]() P4O10(s) ΔH1=-745.8 kJ·mol-1
P4O10(s) ΔH1=-745.8 kJ·mol-1
②4P(s,红橉)+5O2(g)=P4O10(s) ΔH2=-2954 kJ·mol-1
(1)白磷和红磷的关系是_____________。
a.同一种物质 b.同位素 c.同分异构体 D.同素异形体
(2)红磷的燃烧热是________kJ·mol-1,白磷的燃烧热比红磷的燃烧热___________(填“大”或“小”)。
(3)白磷转化为红磷的热化学方程式为P4(s,白磷)=4P(s,红磷)ΔH=-29.2 kJ/mol。在相同的条件下,能量较低的是________(填“白磷”或“红磷”),白磷的稳定性比红磷________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化必须加入氧化剂且通过一步反应就能完成的是( )
①N2→NO2 ②NO2→NO ③NO2→HNO3 ④N2→NO ⑤N2→NH3
A.① B.②⑤
C.④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列说法不正确的是( )
A. 铝热反应可用于冶炼某些金属 B. 聚乙烯和聚氯乙烯可用降解法处理
C. 丁达尔效应可用于区分白酒和淀粉溶液 D. 电渗析法、蒸馏法、离子交换法可用于淡化海水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为六种短周期主族元素,它们的原子序数依次增大;A元素的原子半径最小;B元素原子的最外层电子数是次外层电子数的3倍;C与A同主族,且与E同周期;E元素的最外层电子数是次外层电子数的0.75倍,D既可与C的最高价氧化物的水化物反应,也可与E的最高价氧化物的水化物反应,均有A元素的单质生成。请回答下列问题:
(1)写出F的元素名称_______________,元素B在周期表中的位置_______________。
(2)判断C、D、E离子半径的从大到小顺序________________,比较B和E的气态氢化物的稳定性大小______________________。
(3)写出单质D与C的最高价氧化物的水化物反应的离子方程式___________________。
(4)写出B与C按1:1形成化合物的电子式______________________,用电子式表示B与C按1:2形成化合物的过程_________________
(5)由A、B、C、E四种元素共同构成的两种化合物在溶液中相互间可发生化学反应,试写出该反应的离子方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使用新型电极材料,以N2、H2为电极反应物,以HC1-NH4C1为电解质溶液,可制造出一种既能提供电能,又能实现氮固定的新型燃料电池,原理如下图所示。下列有关分析正确的是( )
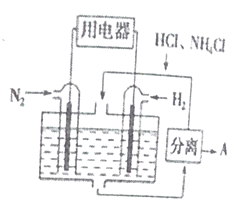
A. 通入H2—极为正极 B. 分离出的物质X为HC1
C. 电池工作一段时间后,溶液pH减小 D. 通入N2一极的电极反应式为:N2+6e-+8H+=2NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】14g铜银合金与足量的某浓度的硝酸反应,将放出的气体与1.12L(标况下)的O2混合,通入水中,恰好被全部吸收,则合金中铜的质量为( )
A. 1.4g B. 2.4g C. 3.2g D. 6.4g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com