
���� ��1���ÿ�ȸʯ���õ����������ɵ�CO2�����ʵ�����Ϊ4��1��ʯ��Ϊ3��1��������Ӧ��aCuCO3•bCu��OH��2+��2a+2b��HCl�T��a+b��CuCl2+aCO2��+��a+2b��H2O���������ѧ��ɿɱ�ʾΪaCuCO3•bCu��OH��2��a��b��ϵ���ٸ���a��bΪ��������a��2��b��2�������������
��2�������ᷢ����Ӧ��aCuCO3•bCu��OH��2+��2a+2b��HCl�T��a+b��CuCl2+aCO2��+��a+2b��H2O�����ȷֽⷴӦ����Ϊ��aCuCO3•bCu��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$��a+b��CuO+aCO2��+bH2O�����ݷ���ʽ������ɵĶ�����̼��CuO�������з��̼�����
��3�����ݶ�����̼�������CuCO3��������ԭ���غ����CuO����С������
��4�����ݶ�����̼�������CuCO3��������CuO��������Cu��OH��2�������������غ����̼������ͭ���������
��� �⣺��1�����ݿ�ȸʯ���õ����������ɵ�CO2�����ʵ�����Ϊ4��1��
��ѧ����ʽaCuCO3•bCu��OH��2+��2a+2b��HCl�T��a+b��CuCl2+aCO2��+��a+2b��H2O
��֪��2��a+b����a=4��1���ɵ�x��y=1��1��
��Ϊx��yΪ��������x��2��y��2��
���Կ�ȸʯ�Ļ�ѧʽ�ɱ�ʾΪCuCO3•Cu��OH��2��
��ʯ�����Ӧ��aCuCO3•bCu��OH��2+��2a+2b��HCl�T��a+b��CuCl2+aCO2��+��a+2b��H2O��ʯ����õ����������ɵ�CO2�����ʵ�����Ϊ3��1����2a+b����x=3��1�����a=2b��
��Ϊx��yΪ��������x��2��y��2����a=2��b=1��
����ʯ��Ļ�ѧʽ�ɱ�ʾΪ2CuCO3•Cu��OH��2��
�ʴ�Ϊ��CuCO3•Cu��OH��2��2CuCO3•Cu��OH��2��
��2��������ʹA��Ʒ��ȫ�ܽ⣬����CO23.36L����״��������n��CO2���T0.15mol��
������Ʒʹ����ȫ�ֽ⣬�õ�20g CuO����n��CuO��=$\frac{20g}{80g/mol}$=0.25mol��
�����ᷢ����Ӧ��aCuCO3•bCu��OH��2+��2a+2b��HCl�T��a+b��CuCl2+aCO2��+��a+2b��H2O��
���ȷֽⷴӦ����Ϊ��aCuCO3•bCu��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$��a+b��CuO+aCO2��+bH2O��
���ϵʽΪ��aCuCO3•bCu��OH��2��aCO2����a+b��CuO
a a+b
0.15mol 0.25mol
����a��b=3��2���ÿ����Ļ�ѧ���ΪCuCO3•Cu��OH��2��2CuCO3•Cu��OH��2�Ļ���
�ʴ�Ϊ���ÿ����Ļ�ѧ���ΪCuCO3•Cu��OH��2��2CuCO3•Cu��OH��2�Ļ���
��3��ij̼������ͭ����aCuCO3•bCu��OH��2��a��bΪ����������a��2��b��2��������ȫ�ܽ����CO2 6.72L����״��������n��CO2��=$\frac{6.72L}{22.4l/mol}$=0.3mol��
aCO2 ����a+b��CuO
0.3mol n��CuO��
n��CuO��=$\frac{0.3��a+b��}{a}$mol����b=1��a=2ʱ����n��CuO������Сֵ��
��CuO������Ϊ$\frac{0.3��a+b��}{a}$mol��80g/mol=0.45mol��80g/mol=36g��
���Էݿ�����CuO����������36g��
�ʴ�Ϊ��36��
��4��������ȫ�ܽ����CO2�������״����ΪV L����n��CO2��=$\frac{V}{22.4}$mol����CԪ���غ��֪��n��CuCO3��=$\frac{V}{22.4}$mol��
����CuO����ΪG g����n��CuO��=$\frac{G}{80}$mol������Cu��OH��2�����ʵ���Ϊ$\frac{G}{80}$mol-$\frac{V}{22.4}$mol��
�������غ��֪A=$\frac{V}{22.4}$mol��124g/mol+��$\frac{G}{80}$mol-$\frac{V}{22.4}$mol����98g/mol=$\frac{124V}{22.4}+98����\frac{G}{80}-\frac{V}{22.4}��$g��
�ʴ�Ϊ��$\frac{124V}{22.4}+98����\frac{G}{80}-\frac{V}{22.4}��$��
���� ���⿼�黯ѧʽ���ƶϡ���ѧ��Ӧ����ʽ�ļ��㣬ע����ݷ���ʽ���м�������Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͼ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
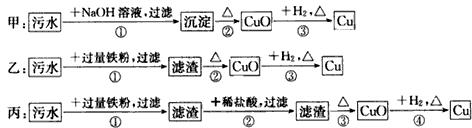
| A�� | ����ʵ�鷽���ж����Ƶô���ͭ | |
| B�� | �����еķ�Ӧ�漰�û����ֽ⡢���ֽ����ַ�Ӧ���� | |
| C�� | �ҷ����мӹ�������ֻ�ܻ�ԭ���еĶ��������� | |
| D�� | �������������������Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
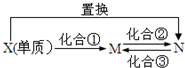 M��NΪ��XԪ�صij������������֮������ͼ��ת����ϵ������˵����ȷ���ǣ�������
M��NΪ��XԪ�صij������������֮������ͼ��ת����ϵ������˵����ȷ���ǣ�������| A�� | X������Mg��CuԪ�� | |
| B�� | ���Ϣڢ۵ķ�Ӧ�����Ƿ�������ԭ��Ӧ | |
| C�� | ��XΪCԪ�أ����ת����ϵ��X���ʷ������û���Ӧ������2C+SiO2$\frac{\underline{\;����\;}}{\;}$Si+2CO | |
| D�� | ��XΪFeԪ�أ���M��H218O��Һ�м������Na2O2�ķ�ӦΪ��4Fe3++6H218O+6Na2O2�T4Fe��OH��3��+12Na++318O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
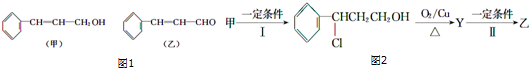
| ����ʽ | C16H14O2 |
| �������� | ��ʹBr2/CCl4��ɫ |
| ����ϡH2SO4��ˮ�� |
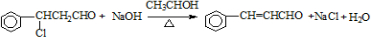 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
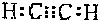 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | [Cl-]��[NH4+]��[H+]��[OH-] | B�� | [Cl-]��[H+]��[NH4+]��[OH-] | C�� | [NH4+]��[OH-]��[Cl-]��[H+] | D�� | [OH-]��[H+]��[Cl-]��[NH4+] |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����C���� | |
| B�� | �������������Сһ�� | |
| C�� | ����������䣬����һ������H2O��g�� | |
| D�� | ����ѹǿ���䣬����N2ʹ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | NaOH/mol•L-1 | HA/mol•L-1 | �����Һ��pH |
| �� | 0.1 | 0.1 | pH=9 |
| �� | c | 0.2 | pH=7 |
| �� | 0.1 | 0.2 | pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �Ĵ����зḻ�Ŀ����Դ�������ѿ���������ֿ������λ��ȫ����1λ���ش��������⣺
�Ĵ����зḻ�Ŀ����Դ�������ѿ���������ֿ������λ��ȫ����1λ���ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com