
| A. | 漂粉精 | B. | 氨气 | C. | 烧碱 | D. | 纯碱 |
分析 有电子转移的化学反应是氧化还原反应,其特征是有元素化合价的变化,据此对各选项进行判断.
解答 解:A.制漂粉精的反应为2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,反应中存在单质参加反应或生成,属于氧化还原反应,故A不选;
B.工业制用氮气与氢气反应制取氨气,属于氧化还原反应,故B不选;
C.工业制取烧碱涉及的反应为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2NaOH,该反应中有电子的转移,属于氧化还原反应,故C不选;
D.氨碱法生产纯碱涉及的方程式为:NH3+CO2+H2O+NaCl═NaHCO3+NH4Cl、2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,这几个方程式中都没有电子的转移,所以不涉及氧化还原反应,故D选;
故选D.
点评 本题考查了化学反应方程式的书写,明确物质的性质是解本题关键,注意掌握氧化还原反应的实质与特征,试题有利于提高学生的分析能力及灵活应用能力.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:实验题
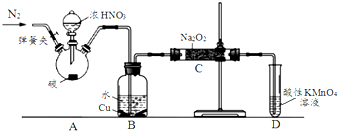
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
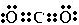 ,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.
,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.| 共价键 | H-H | H-F | H-Cl | H-Br | H-O | H-S | H-N | H-P |
| 键长(pm) | 74 | 92 | 127 | 141 | 98 | 135 | 101 | 321 |
| 键能(kJ/mol) | 436 | 568 | 432 | 368 | 464 | 364 | 391 | 142 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是一种化学活性很高的烃,存在于煤焦油中.
)是一种化学活性很高的烃,存在于煤焦油中. $\stackrel{室温}{→}$
$\stackrel{室温}{→}$ ,反应类型为加成;该反应的产物除
,反应类型为加成;该反应的产物除 外,还有与双环戊二烯为同分异构体的其他副产物,写出其中一种的结构简式
外,还有与双环戊二烯为同分异构体的其他副产物,写出其中一种的结构简式 ;
; )是双环戊二烯的一种同分异构体,它的一氯代物有4种.
)是双环戊二烯的一种同分异构体,它的一氯代物有4种.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
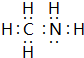 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | BaCl2溶液 | B. | Ba(NO3)2溶液 | C. | 浓溴水 | D. | 饱和NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
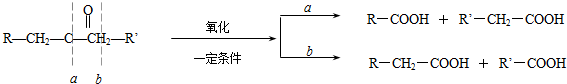
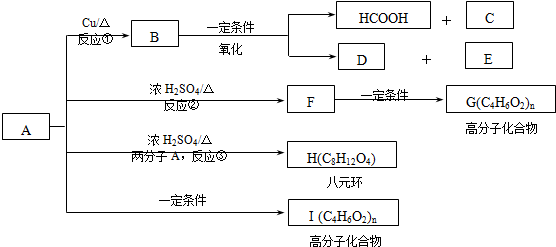
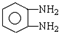 )生成一种合成纤维:
)生成一种合成纤维: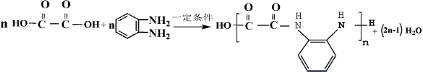 .
.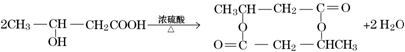 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4 | B. | C3H8 | C. | C4H8 | D. | C5H10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com