
��֪��Ԫ��������ϼۣ��仯�ϼ���һ3��0��+1��+2��+3��+4��+5
��1���±���������ij�ֽ���M��ijЩ�����·�Ӧ���û�ԭ����Ĺ�ϵ��
����п��ijŨ�ȵ����ᷴӦʱ���������������˻�ѧ��Ӧ�б���ԭ��������μӷ�Ӧ���������ʵ���֮����____________��
��2������Ϊȼ�ϵĹ������������02��)ȼ�ϵ�أ�����ȫ��̬�ṹ������Ч�ʸߡ�����Ⱦ���ص㣬���ⰱ���������ߣ�����̼����Һ����������������棬�Ǻܺõ���Դ���塣�乤��ԭ����ͼ��ʾ��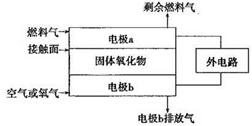
�ٸõ�ع���ʱ���ܷ�ӦΪ_______________________
�ڹ�����������Ϊ��ع����ĵ���ʣ�O2-�ƶ�����Ϊ________(ѡ��ɵ缫a��缫b�����ɵ缫b��缫a��)��
�۸õ�ع���ʱ���ڽӴ����Ϸ����ĵ缫��ӦΪ________��
��3��N2O5��һ�������������������ʺ��Ʊ��ܵ����ǵĹ�ע����ͼ��ʾװ�ÿ������Ʊ�N2O5,д���ڵ���������N2O5�ĵ缫��Ӧʽ________________��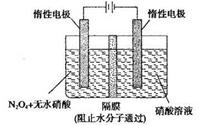
��1��1��10 4Zn+10HNO3(ϡ)=4Zn(NO3) 2+NH4NO3+3H2O����2��4NH3+3O2=2N2+6H2O.�ɵ缫b��缫a(��Ϊ��������ԭ��صĸ����ƶ�) 2NH3+3O2-+6e-= N2+3H2O ��3��N2O4+2HNO3-2e-=2N2O5+2H+��
���������������1������п��ijŨ�ȵ����ᷴӦʱ�������������˵�����ᱻ��ԭ�����İ������������ղ���������李���Ӧ�Ļ�ѧ����ʽΪ��4Zn+10HNO3(ϡ)=Zn(NO3) 2+NH4NO3+3H2O�˻�ѧ��Ӧ����10��HNO3�μӷ�Ӧ�����б���ԭ��HNO3��1�������Ա���ԭ��������μӷ�Ӧ���������ʵ���֮����1��10.��2���ٸõ�ع���ʱ���ܷ�ӦΪ4NH3+3O2=2N2+6H2O���� ������������Ϊ��ع����ĵ���ʣ�O2-��������ɽ϶�ĸ��������ƶ������ƶ�����Ϊ�ɵ缫b��缫a���۸õ�ع���ʱ���ڽӴ����Ϸ����ĵ缫��ӦΪ2NH3+3O2-+6e-= N2+3H2O ����3���õ�ⷨ��N2O4��2HNO3Ϊԭ�ϣ��ڵ���������N2O5�ĵ缫��ӦʽN2O4+2HNO3-2e-=2N2O5+2H+��
���㣺��������Ļ�ѧ���ʼ�Ӧ�á�����ȼ�ϵ�صĹ���ԭ����֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ͭ��������������Ԫ�أ�Ҳ����������ʹ�õĽ���֮һ��ͭ��������ʹ�öԹ��������������涼��������Զ��Ӱ�졣
��1��д��ͭ��ϡ���ᷴӦ�Ļ�ѧ����ʽ��________________________________________________________________________________________________________________________________________________��
��2��Ϊ�˱��������ͽ�Լ��Դ��ͨ������H2O2��ϡ����Ļ����Һ�ܳ��Ͼ�ӡˢ��·���е�ͭ������ʵ��ͭ�Ļ������á�д���ܳ�ͭ�����ӷ���ʽ��________________________________________________________________________________________________________________________________________________��
��3����ҵ���Ի�ͭ��Ϊԭ�ϣ����û�������������ͭ���ù��յ��м���̻ᷢ����Ӧ��2Cu2O��Cu2S 6Cu��SO2�����÷�Ӧ����������______________��������19.2 g Cuʱ����Ӧ��ת�Ƶĵ���Ϊ__________mol��
6Cu��SO2�����÷�Ӧ����������______________��������19.2 g Cuʱ����Ӧ��ת�Ƶĵ���Ϊ__________mol��
��4��ͭ�ڳ�ʪ�Ŀ������ܷ���������ʴ�����⣬ͭ�����Ҫ�ɷ�ΪCu2��OH��2CO3����ʽ̼��ͭ������д�����������и����ĵ缫��Ӧʽ��________________________________________________________________________________________________________________________________________________��
��5���о���ѧϰС���á���ӵ��������ⶨij����CuSO4��5H2O����������I����Ӧ�����������ʣ��ĺ�����ȡa g�������100 mL��Һ��ÿ��ȡ25.00 mL���μ�KI��Һ���а�ɫ�⻯��������ɡ�д���÷�Ӧ�����ӷ���ʽ��___________________________�������μ�KI��Һ���������ٲ�������Һ�е�I2����������Ʊ���Һ�ζ���������Ӧ�Ļ�ѧ����ʽΪI2��2Na2S2O3=2NaI��Na2S4O6��ƽ������c mol/L��Na2S2O3��ҺV mL����������CuSO4��5H2O����������Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1�����÷�Ӧ��6NO2��8NH3 7N2��12H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״���µ������ L��
7N2��12H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״���µ������ L��
��2������֪��2SO2(g)+O2(g) 2SO3(g) ��H��?196.6 kJ��mol�C1
2SO3(g) ��H��?196.6 kJ��mol�C1
2NO(g)+O2(g) 2NO2(g) ��H��?113.0 kJ��mol�C1
2NO2(g) ��H��?113.0 kJ��mol�C1
��д��NO2��SO2��Ӧ����SO3(g)��NO���Ȼ�ѧ����ʽ ��
��һ�������£���NO2��SO2�������1:2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ��� d��ÿ����1 mol SO2��ͬʱ����1 molNO2
�۲��������Ӧƽ��ʱNO2��SO2�����Ϊ1:6����÷�Ӧ��ƽ�ⳣ��K�� ��
��3������β���е�һ����̼��ͨ�����·�Ӧ������Ũ�ȣ�CO(g)+1/2O2(g) CO2(g)����֪ij�¶��£������������ܱ������н��и÷�Ӧ�������и����ʵ���ʼŨ�ȼ������淴Ӧ���ʹ�ϵ���±���ʾ�����á���������������д���еĿո�
CO2(g)����֪ij�¶��£������������ܱ������н��и÷�Ӧ�������и����ʵ���ʼŨ�ȼ������淴Ӧ���ʹ�ϵ���±���ʾ�����á���������������д���еĿո�
| ������� | c(CO)��mol��L�C1 | c(O2)��mol��L�C1 | c(CO2)��mol��L�C1 | ��(��)�ͦ�(��) ��С�Ƚ� |
| �� | 2.0��10�C4 | 4.0��10�C4 | 4.0��10�C4 | ��(��)����(��) |
| �� | 1.0��10�C3 | 4.0��10�C4 | 5.0��10�C4 | ��(��) ��(��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������������Դ�������ȷ������Ź㷺����;��ʪ�����ɷ��Ʊ��������ε�ԭ�����±���ʾ��
��1����ҵ����ʪ���Ʊ�������أ�K2FeO4������������ͼ��ʾ��
|
 ��ϴ�Ӵ�Ʒʱѡ�������������ˮ�������ǣ� ��
��ϴ�Ӵ�Ʒʱѡ�������������ˮ�������ǣ� ��| ʪ�� | ǿ���Խ����У�Fe(NO3)3��NaClO��Ӧ�����Ϻ�ɫ����������Һ |
| �ɷ� | Fe2O3��KNO3��KOH��ϼ��ȹ��������Ϻ�ɫ�������κ�KNO2�Ȳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��Ԫ�صĻ������ڹ�ũҵ�Լ������Ƽ�����;�㷺����Ҳ��Ի��������Ⱦ�������ˮ����������ɵĵ���Ⱦ�ѳ�Ϊһ�������ԵĻ������⡣
���������գ�
��1��ij������ģ�����ˮ�ѵ����̣�����Fe�ۺ�KNO3(aq)��Ӧ̽���ѵ�ԭ����ʵ��ǰ
����0.1mol��L-1H2SO4(aq)ϴ��Fe�ۣ���Ŀ���� ��Ȼ��������ˮϴ�������ԣ�
�ڽ�KNO3(aq)��pH����2.5��
��Ϊ��ֹ�����е� ��д��ѧʽ�����ѵ���Ӱ�죬Ӧ��KNO3��Һ��ͨ��N2��
��2��������Fe�ۻ�ԭ����KNO3(aq)�����У���Ӧ���������������Ũ�ȡ�pH��ʱ��ı仯��ϵ��ͼ��ʾ�������ͼ����Ϣд��t1ʱ��ǰ�÷�Ӧ�����ӷ���ʽ�� ��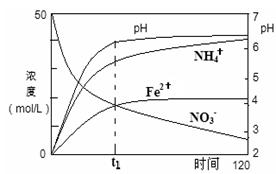
��3���������˷ɴ��Ļ���ƽ����г����£�N2H4����ȼ�ϡ�NH3��NaClO��Ӧ�ɵõ��£�N2H4�����÷�Ӧ�б������뱻��ԭ��Ԫ�ص�ԭ�Ӹ���֮��Ϊ �������Ӧ����5mol���ӷ���ת�ƣ��ɵõ��� g��
��4����������25mL 0.01mol/Lϡ�����л���ͨ��5.6 mL NH3����״������Һ����仯���Բ��ƣ�����Ӧ����Һ������Ũ���ɴ�С��˳���� ����ͨ��NH3�Ĺ�������Һ�ĵ������� ����д���������С���������䡱����
��5����������Һ�м���ͨ��NH3���ù���������Ũ�ȴ�С��ϵ������ȷ���� ��ѡ���ţ���
a��c(Cl-)=c(NH4+)��c(H+)=c(OH-) b��c(Cl-)��c(NH4+)=c(H+)��c(OH-)
c��c(NH4+)��c(OH-)��c(Cl-)��c(H+) d��c(OH-)��c(NH4+)��c(H+)��c(Cl-)
��6����������25mL��HCl 0.01mol����Һ�еμӰ�ˮ���������ù�����ˮ�ĵ���ƽ�� ����д����ƽ���ƶ�����������μӰ�ˮ��25mLʱ�������Һ��ˮ�ĵ���������ˮ��Ũ��Ϊ mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ϳɰ����Ʊ�������������Ҫ�Ļ�������������ij���������ϳɰ����Ʊ������������������
��1����ij�¶������Ϊ200 L�İ��ϳ����У��Է�Ϊ��λ��ʱ����ϲ�ø����ʵ�Ũ��(mol��L��1)���±���
| | 0 min | l min | 2 min | 3 min | 4 min |
| N2 | 1.500 | 1.400 | 1.200 | c1 | c1 |
| H2 | 4.500 | 4.200 | 3.600 | c2 | c2 |
| NH3 | 0 | 0.200 | 0.600 | c3 | c3 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���ֹ�������ˮ������ɱ����Ϊ���ƴ��ģ��Ⱦ�Լ�����������Ч����֮һ��
Ư���dz��õ�����������ҵ�Ͻ�����ͨ��ʯ����[Ca(OH)2]��ȡƯ�ۣ���ѧ��Ӧ����ʽΪ ��Ư�۵���Ч�ɷ��ǣ��ѧʽ�� ���÷�Ӧ���������뻹ԭ�����ʵ���֮���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1����ƽ�÷�Ӧ���������ת�Ƶķ������Ŀ��KMnO4��HCl = MnCl2�� KCl�� Cl2���� H2O
��2����������________________������������__________________(�ѧʽ)��
��3��������71 g Cl2���ĵ�HCl��___________________����������HCl��_______________��
��4��CS2��Һ�壩����O2����ȫȼ�գ�����CO2��SO2������0.1 mol CS2��1 mol O2����ȫȼ�գ����û�������ڱ�״������ռ�����Ϊ__________L��
��(6��)��1������A. B. C. D������ѧ�����Ļ���������ᴿ�Ļ���װ��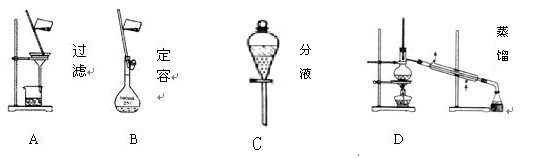
�����ʵ����Ҫ��A. B.C. Dװ�������ʵ��Ŀո��С�
�ٷ������ͺ��Ȼ�����Һ____________________
��������ˮ��ȡ����ˮ__________________
�۳�ȥ������Һ����������ɳ_______________________________
��2������Fe3+���õ��Լ������⣬�����Խ�KSCN��Һ����������Һ�У��������������______
________________________��������Ӧ�����ӷ���ʽ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1����ͼ�ǿα��С����ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��ͼ����H2+CuO  Cu+H2O����Ӧ����ͼ�е����� ������ţ������з�Ӧ����������7���� ��
Cu+H2O����Ӧ����ͼ�е����� ������ţ������з�Ӧ����������7���� ��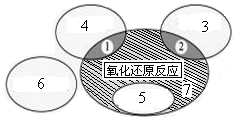
A��2H2+O2 2H2O 2H2O |
B��2NaHCO3 Na2CO3+H2O+CO2�� Na2CO3+H2O+CO2�� |
| C��Zn+H2SO4=ZnSO4+H2�� |
D��CuO+CO Cu+CO2 Cu+CO2 |
 N2+6NH4Cl
N2+6NH4Cl�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com