
【题目】实验室用硼镁泥为原料制取MgSO4·7H2O粗产品的过程如下:
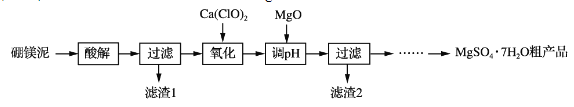
硼镁泥的主要成分如下表:
MgO | SiO2 | FeO、Fe2O3 | CaO | Al2O3 | B2O3 |
30%~40% | 20%~25% | 5%~15% | 2%~3% | 1%~2% | 1%~2% |
(1)“酸解”时为提高Mg2+的浸出率,可采用的措施是_____(写一种)。所加酸不宜过量太多的原因是_____。
(2)“氧化”步骤中,若用H2O2代替Ca(ClO)2,则发生反应的离子方程式为______________。实际未使用H2O2,除H2O2成本高外,还可能的原因是______________________________________。
(3)“调pH”时用MgO而不用NaOH溶液的原因是________________________。
(4)结合附表信息,由MgSO4·7H2O粗产品(含少量CaSO4)提纯获取MgSO4·7H2O的实验方案如下:将粗产品溶于水,_________________________________________________,室温下自然挥发干燥。(实验中必须使用的试剂有:饱和MgSO4溶液,乙醇)附:两种盐的溶解度(g/100 g水)
温度℃ | 10 | 30 | 40 | 50 |
CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 |
MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 |
【答案】加热/搅拌/提高酸液浓度等避免调pH时消耗过多的MgOH2O2+2Fe2++2H+===2Fe3++2H2OH2O2不稳定易分解或Fe3+等金属离子会催化H2O2的分解防止加入的NaOH引入Na+杂质加热浓缩,趁热过滤;将滤液冷却结晶,过滤,用饱和MgSO4溶液洗涤,再用乙醇洗涤
【解析】
(1)为加快反应速率,可以采用升高温度、适当增大反应物浓度、增大反应物接触面积等方法,如适当升高温度、把硼镁泥粉碎、或搅拌、或适当增加硫酸浓度;另外所加酸过量太多,在后续操作中消耗过多的MgO,故答案为:加热/搅拌/提高酸液浓度等;避免调pH时消耗过多的MgO;
(2)“氧化”步骤主要是氧化亚铁离子,方便通过调节pH而将铁元素除去,方程式为:H2O2+2Fe2++2H+===2Fe3++2H2O;但双氧水不稳定,易分解,其中Fe3+为其分解的催化剂,因此不宜用H2O2代替Ca(ClO)2,故答案为:H2O2+2Fe2++2H+===2Fe3++2H2O、H2O2不稳定易分解或Fe3+等金属离子会催化H2O2的分解;
(3)用MgO来调节溶液的pH时,即使过量,也易通过过滤而除去,且不引入新的杂质,故答案为:防止加入的NaOH引入Na+杂质;
(4)由CaSO4和MgSO4·7H2O溶解的特点可知,宜采用冷却结晶的办法来除去CaSO4,然后用饱和MgSO4溶液洗涤除去杂质,用乙醇洗涤利于去除水分,故答案为:加热浓缩,趁热过滤;将滤液冷却结晶,过滤,用饱和MgSO4溶液洗涤,再用乙醇洗涤。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知烃B分子内C、H原子个数比为1:2,相对分子质量为28,核磁共振氢谱显示分子中只有一种化学环境的氢原子,且有如下的转化关系:

(1)B的结构简式是_________________;
(2)A可能属于下列哪类物质__;
a.醇 b.卤代烃 c.酚 d.羧酸
(3)反应①是D与HCl按物质的量之比1:1的加成反应,则D的分子式是_____________,反应②可表示为:G+NH3→F+HCl (未配平),该反应配平后的化学方程式是____________(有机化合物均用结构简式表示);
化合物E(HOCH2CH2Cl)和 F[HN(CH2CH3)2]是药品普鲁卡因合成的重要中间体,普鲁卡因的合成路线如下:(已知: )
)
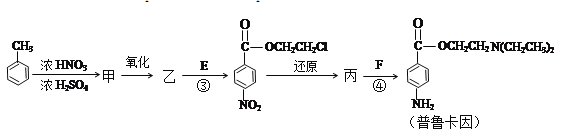
(4)甲的结构简式是__,由甲苯生成甲的反应类型是__;
(5)乙中有两种含氧官能团______,反应③的化学方程式是:______;
(6)丙中官能团的名称是______;
(7)普鲁卡因有两种水解产物丁和戊;
①戊与甲互为同分异构体,戊的结构简式是__;
②戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域.该聚合反应的化学方程式是__;
③D的红外光谱表明分子内除C﹣H键、C﹣C键外还含有两个C﹣O单键.则D与F在一定条件下反应生成丁的化学方程式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应能用离子方程式:H++OH-=H2O。表示的是( )
A.CH3COOH+NaOH=CH3COONa+H2O
B.2H2SO4+Cu(OH)2=CuSO4+2H2O
C.HCl+KOH=KCl+H2O
D.HCl+NH3·H2O=NH4Cl+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图虚线框中的装置可用来检验浓硫酸与木炭粉的加热条件下反应产生的所有气体产物,填写下列空白:
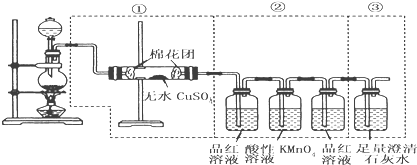
(1)如果装装置中①、②、③三部分仪器的连接顺序改为②、①、③,则可以检出的物质是____________;不能检出的物质是____________。
(2)如果将仪器的连接顺序变为①、③、②,则可以检出的物质是____________;不能检出的物质是____________。
(3)如果将仪器的连接顺序变为②、③、①,则可以检出的物质是____________;不能检出的物质是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
![]()
(1)写出A、B、C三元素名称________、________、________。
(2)C在元素周期表中的位置是____________________。
(3)B的原子结构示意图为________________,C的氢化物与B的氢化物的稳定性强弱顺序为________>________(填化学式)。
(4)比较A、C的原子半径A________C,写出A的气态氢化物与A的最高价氧化物对应水化物反应的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有Al、C12、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )
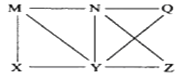
A. N一定是HCl(aq) B. X可能为Al或C12
C. Y一定为NaOH(aq) D. Q、Z中的一种必定为Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 不同的离子化合物所含的化学键相同
B. 离子键是阴阳离子间的静电吸引
C. 同素异形体之间的相互转化是化学变化,
D. 非金属元素形成的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施对增大反应速率有效的是:
A. Fe与稀硫酸反应制取H2时,改用浓硫酸
B. Na与水反应时增大水的用量
C. 在K2SO4与BaCl2两溶液反应时,增大压强
D. 密闭容器中进行的反应:C+O2![]() CO2,增大压强
CO2,增大压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com