
| A. | 向某溶液中加入氯水再滴加KSCN溶液,溶液呈红色,说明原溶液中含有Fe2+ | |
| B. | 取某溶液进行焰色反应,透过蓝色钻玻璃焰色为紫色,则原溶液的溶质一定是KNO3 | |
| C. | 向某溶液中加入BaCl2溶液,生成白色沉淀,再加入稀盐酸,沉淀不溶解,则原溶液不一定含有SO42- | |
| D. | 往Na2CO3和NaHCO3溶液中滴加酚酞都变红,说明Na2CO3和NaHCO3都是碱 |
分析 A.先加氯水可氧化亚铁离子;
B.焰色反应为元素的性质;
C.白色沉淀可能为AgCl或硫酸钡;
D.滴加酚酞都变红,可知水解是溶液显碱性.
解答 解:A.先加氯水可氧化亚铁离子,干扰亚铁离子检验,则检验亚铁离子时先加KSCN溶液无现象、后加氯水变血红色,故A错误;
B.焰色反应为元素的性质,则焰色为紫色,则原溶液的溶可能是KNO3、KOH等,一定含K元素,故B错误;
C.白色沉淀可能为AgCl或硫酸钡,则再加入稀盐酸,沉淀不溶解,则原溶液不一定含有SO42-,可能含银离子,但不能同时存在,故C正确;
D.滴加酚酞都变红,可知水解是溶液显碱性,Na2CO3和NaHCO3均为强碱弱酸盐,故D错误;
故选C.
点评 本题考查常见离子的检验,为高频考点,把握离子检验的试剂、现象、结论为解答的关键,侧重分析与实验能力的考查,注意排除干扰离子的影响,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2 (g)+O2(g)=2H2O(l) | B. | H2(g)+Cl2 (g)=2HCl(g) | ||
| C. | (NH4)2CO3(s)=NH4HCO3 (s)+NH3(g) | D. | Cu(s)+Cl2 (g)=CuCl2 (s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
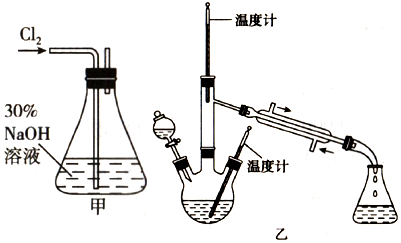 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O):
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①中,负极上消耗1 mol甲醛时转移2 mol电子 | |
| B. | ①溶液中的H+由正极移向负极 | |
| C. | 理论上消耗的甲醛与生成的Fe2+的物质的量之比为1:4 | |
| D. | ④中,甲醛浓度越大,吸光度越小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NaHCO3固体加入新制氯水中,有无色气泡(H+) | |
| B. | 新制氯水呈黄绿色(Cl2) | |
| C. | 使蓝色石蕊试纸先变红后褪色(H+、Cl2) | |
| D. | 滴加AgNO3溶液生成白色沉淀(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
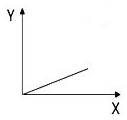
| A. | 一定状况下,气体摩尔体积(Y)与该气体的物质的量(X)的关系 | |
| B. | 在光照情况下,一定体积的饱和氯水的pH(Y)随时间(X)的关系 | |
| C. | 100℃,1个大气压下,按体积比1:1混合的CO2和H2O(g)混合气通过足量Na2O2粉末,固体增加的质量(Y)与混合气体积(X)的关系 | |
| D. | 向AlCl3溶液中滴加NaOH溶液至过量,生成Al(OH)3 的物质的量(Y)与消耗NaOH的物质的量(X)的关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大反应物浓度,可增大单位体积内活化分子的百分数 | |
| B. | 对于有气体参加的化学反应,若增大压强,可增大活化分子的百分数 | |
| C. | 升高温度,可以增大活化分子百分数 | |
| D. | 活化分子间的碰撞一定是有效碰撞 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8:5 | B. | 6:5 | C. | 2:1 | D. | 1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com