
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如下的转化关系(部分产物及反应条件已略去),下列判断正确的是

A.X元素可能为Al B.X元素一定为非金属元素
C.反应①和②互为可逆反应 D.反应①和②可能为氧化还原反应
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源:2014-2015湖北省襄阳市四校高二12月联考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.常温下,反应C(s) + CO2(g)=2CO(g)不能自发进行,则该反应△H>0
B.强电解溶液的导电能力一定强于弱电解质溶液的导电能力
C.CH3COOH、Cu(OH)2、BaSO4、NH3都是常见的弱电解质
D.常温下就能发生的化学反应一定是放热反应
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一12月月考化学试卷(解析版) 题型:选择题
下列物质性质的比较叙述正确的是
A.在水中溶解性:Na2CO3<NaHCO3
B.热稳定性:Na2CO3>NaHCO3
C.同浓度溶液与足量酸反应的速度:Na2CO3>NaHCO3
D.将固体溶于少量水放出的热量:Na2CO3<NaHCO3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省建人高复高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列图示与对应的叙述不相符的是
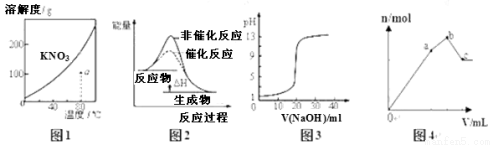
A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1醋酸溶液得到滴定曲线
D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省建人高复高三上学期第三次月考化学试卷(解析版) 题型:选择题
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是
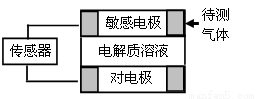

A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2时,敏感电极的电极反应式为:Cl2 + 2e-= 2Cl-
C.检测H2S时,对电极充入空气,对电极上的电极反应式为O2 + 2H2O+ 4e- = 4OH-
D.检测分别含H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省建人高复高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列说法或表示方法正确的是
A.己知2C(s)+2O2(g)=2CO2(g);△H1 2C(s)+O2(g)=2CO(g);△H2 则△H1>△H2
B.在稀溶液中:H+(aq)+OH﹣(aq)=H2O(l);△H=﹣57.3kJ/mol,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量
C.由C(石墨)=C(金刚石);△H=+1.9 kJ/mol,可知金刚石比石墨稳定
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=﹣285.8kJ/mol;
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期第三次月考化学试卷(解析版) 题型:实验题
(10分)某同学帮助水质检测站配制800mL 1 mol·L-1NaOH溶液备用。
(1)该同学应选择的玻璃仪器除了烧杯、量筒、玻璃棒、胶头滴管外,还有 。

(2)其操作步骤如下图所示,则如图操作应在下图中的 (填选项字母)之间。
A.②与③ B.①与② C.④与⑤ D.③与④
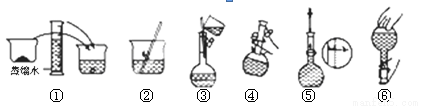
(3)该同学应用托盘天平称取NaOH固体 g,用质量为33.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在下图中选出能正确表示游码位置的选项 (填选项字母)。

(4)下列操作对所配溶液浓度大小有何影响 (填“偏大”、“偏小”或“无影响”)。
①定容时,仰视读数,浓度会 ;
②转移溶液过程中,未洗涤玻璃棒和烧杯,浓度会 ;
③容量瓶未干燥,浓度会 ;
④定容摇匀后发现溶液凹面低于刻度线,继续加水至刻度线,浓度会 。
(5)配制溶液的实际操作过程中,动作要快,否则由于 ,会使配制的NaOH溶液的浓度比1 mol·L-1 ______(填“大”或“小”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期第三次月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,1 mol CO2和CO的混合气中含有的氧原子数为1.5NA
B.常温常压下,33.6 L 氯化氢气体中含有的分子数为1.5NA
C.12g Mg与足量二氧化碳反应转移的电子数为NA
D.1 mol·L-1 CuCl2溶液中含有的氯离子数为2NA
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省乐清市高二上学期10月月考化学试卷(解析版) 题型:选择题
下列关于判断过程的方向的说法正确的是
A.所有自发进行的化学反应都是放热反应
B.判断化学反应能否自发进行,必须综合考虑反应的焓变和熵变
C.自发反应一定是熵增大,非自发反应一定是熵减小的反应
D.同一物质的固、液、气三种状态中固体的熵值最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com