
分析 ①无机非金属材是以某些元素的氧化物、碳化物、氮化物、卤素化合物、硼化物以及硅酸盐、铝酸盐、磷酸盐、硼酸盐等物质组成的材料,一般可认为是有机高分子材料和金属材料以外的所有材料的统称;
②工业炼铁原理用一氧化碳还原铁矿石;
③依据钢铁的腐蚀和防护原理解答.
解答 解:①硬币属于金属材料;聚氯乙烯塑料属于有机高分子材料;氮化硅陶瓷是硅酸盐材料属于无机非金属材料;
故选:C;
②工业炼铁原理用一氧化碳还原铁矿石,方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,
故答案为:工业炼铁原理用一氧化碳还原铁矿石;
③铁锅未及时洗净(残液中含NaCl)能发生电化学腐蚀,由于电解质溶液为中性所以发生吸氧腐蚀;锌比铁还原性强,在海水中形成原电池,锌做负极发生氧化反应,被腐蚀;铁做正极被保护属于牺牲阳极的阴极保护法;
故答案为:吸氧;锌块.
点评 本题考查了生活中常见的材料,金属的腐蚀与防护等方面的知识,题目难度不大,注意知识的积累.


科目:高中化学 来源: 题型:多选题
| A. | SiH4比CH4稳定 | |
| B. | O2-半径比F-的小 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 | |
| D. | 酸性 HClO4>H2SO4>CH3COOH>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
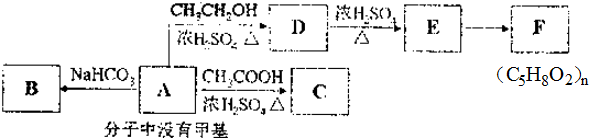
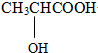 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 参加反应的H2和硝酸的物质的量之比为3:1 | |
| B. | 混合物中氧原子的物质的量为0.3mol | |
| C. | 混合物中铁原子的物质的量为0.3mol | |
| D. | 参加反应的硝酸的物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
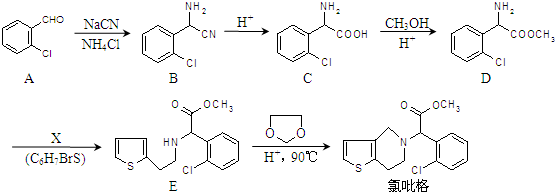
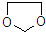 在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式.CH2OHCH2OH$→_{△}^{浓H_{2}SO_{4}}$CH≡CH↑+2H2O
在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式.CH2OHCH2OH$→_{△}^{浓H_{2}SO_{4}}$CH≡CH↑+2H2O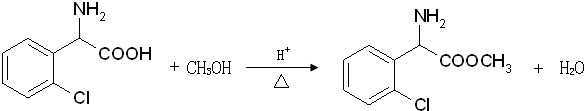
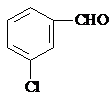 、
、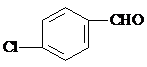 、
、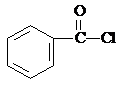 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
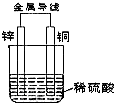 根据如图铜锌原电池示意图,回答下列问题:
根据如图铜锌原电池示意图,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com