
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
科目:高中化学 来源: 题型:解答题
 下面给出了四种烃A、B、C、D的相关信息:
下面给出了四种烃A、B、C、D的相关信息: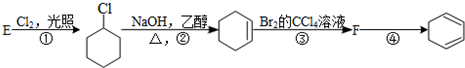
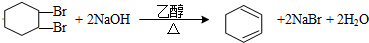 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
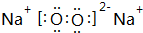 ,其中含有的化学键为离子键、共价键.
,其中含有的化学键为离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H2SO4的酸性比HClO3酸性强 | |
| B. | Fe在纯氧中燃烧生成Fe3O4,Fe在氯气中燃烧生成FeCl3 | |
| C. | 在HClO中,元素化合价氯为+1价,氧为-2价 | |
| D. | O2为无色无味气体,Cl2为黄绿色有刺激性气味的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
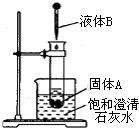 如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入固体试剂A,再在试管中用滴管滴入5mL液体试剂B.可见到烧杯中饱和的澄清石灰水变浑浊.试回答下列问题:
如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入固体试剂A,再在试管中用滴管滴入5mL液体试剂B.可见到烧杯中饱和的澄清石灰水变浑浊.试回答下列问题:| 固体试剂A | 液体试剂B | |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从 IIIB 族到 IIB 族 10 个纵行的元素都是金属元素 | |
| C. | 第ⅠA 族元素的金属性比第ⅡA 族元素的金属性强 | |
| D. | 在周期表里,主族元素所在的族序数等于原子核外电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N 2为0.2 mol•L-1,H 2为0.6 mol•L-1 | |
| B. | N 2为0.15 mol•L-1 | |
| C. | N 2、H 2均为0.18 mol•L-1 | |
| D. | NH 3为0.4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取少量卤代烃加入NaOH水溶液共热,冷却,再加入AgNO3溶液检验卤代烃中卤原子的存在 | |
| B. | 除去乙烷中混有乙烯,将混合气体通入酸性高锰酸钾溶液 | |
| C. | 用燃烧的方法鉴别甲烷与乙炔 | |
| D. | 用溴水鉴别苯和甲苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com