
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是 ( )
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.元素Z、W的简单离子的电子层结构不同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
科目:高中化学 来源: 题型:
反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在容积为10 L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率
4NO(g)+6H2O(g)在容积为10 L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率 (x)(反应物的消耗速率或产物的生成速率)可表示为 ( )
(x)(反应物的消耗速率或产物的生成速率)可表示为 ( )
A. (NH3)=0.010 0 mol·L-1·s-1
(NH3)=0.010 0 mol·L-1·s-1
B. (O2)=0.001 0 mol·L-1·s-1
(O2)=0.001 0 mol·L-1·s-1
C. (NO)=0.001 0 mol·L-1·s-1
(NO)=0.001 0 mol·L-1·s-1
D. (H2O)=0.045 0 mol·L-1·s-1
(H2O)=0.045 0 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.反应热就是反应中放出的能量
B.放热反应在常温下一定很容易发生
C.由C(石墨) C(金刚石) ΔH=+1.9 kJ·mol-1可知,金刚石比石墨稳定
C(金刚石) ΔH=+1.9 kJ·mol-1可知,金刚石比石墨稳定
D.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项表述正确的是 ( )
A.水分子的结构式是H— —H
—H
B.NaCl的电子式为N
C.23Na37Cl中质子数和中子数之比是7∶8
D.三氟化氮的电子式为 F
F
查看答案和解析>>
科目:高中化学 来源: 题型:
Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍。下列说法正确的是 ( )

A.原子半径大小顺序为r(Q)>r(R)>r(T)>r(M)>r(W)
B.Q、W的单核离子的核外电子数相等
C.五种元素均能形成氢化物
D.W的氢化物水溶液酸性最强,说明W的非金属性在五种元素中最强
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等。请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等。请回答下列问题:
(1)T的原子结构示意图为 。
(2)元素的非金属性(原子的得电子能力):
Q W(填“强于”或“弱于”)。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为__________________________________
__________________________________________________________________。
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是_________________________________________________。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化是通过取代反应来实现的是 ( )
A.CH3CH2OH CH3CHO
CH3CHO
B.CH2 CH2
CH2 CH3—CH2Br
CH3—CH2Br
C.CH2 CH2+H2O
CH2+H2O CH3CH2OH
CH3CH2OH
D.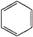


查看答案和解析>>
科目:高中化学 来源: 题型:
最近科学家在-100 ℃的低温下合成了一种烃X,其核磁共振氢谱表明该分子中的氢原子的化学环境没有区别,根据分析,绘制了如图所示的球棍模型。下列说法中错误的是( )
 A.烃X的分子式为C5H4
A.烃X的分子式为C5H4
B.分子中碳原子的化学环境有2种
C.该有机物含有官能团
D.X分子中只有碳碳单键,没有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ. 乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再水解生成乙醇。写出相应反应的化学方程式:
________________________________________________________________________。
(2)已知:
甲醇脱水反应 2CH3OH(g) === CH3OCH3(g) + H2O(g) △H1 == -23.9 kJ·mol—1
甲醇制烯烃反应 2CH3OH(g) === C2H4(g) + 2H2O(g) △H2 == -29.1 kJ·mol—1
乙醇异构化反应 C2H5OH(g) === CH3OCH3(g) △H3 == + 50.7 kJ·mol—1
则乙烯气相直接水合反应C2H4(g) + H2O(g)=== C2H5OH(g)的△H == __________________________。与间接水合法相比,气相直接水合法的优点是__________________________________。
Ⅱ. 甲醇虽然毒性很强,但它是一种清洁燃料,也是一种重要的合成原料。工业甲醇的质量分数可以用下列方法测定:
①在稀硫酸中甲醇被Cr2O72-氧化成CO2和H2O,其反应为:
CH3OH + Cr2O72— + 8H+ ==== CO2↑+ 2Cr3+ + 6H2O;
②过量的Cr2O72—可用Fe2+与之完全反应,反应如下所示:
____Cr2O72— + ____Fe2+ +____H+ ――― ____Cr3+ +____Fe3+ +____H2O
现有0.12 g工业甲醇,在稀硫酸中与25.0 mL 0.2 mol/L K2Cr2O7溶液反应,多余的K2Cr2O7
恰好与9.6 mL 1.0 mol/L FeSO4溶液完全反应。
(3)请配平第②步中离子方程式(配平系数依次填写在短线上)。
(4)工业甲醇的质量分数为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com