
| A、向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体 |
| B、测定工业烧碱的含量(含杂质碳酸钠)可称取一定量样品放人锥形瓶中,加适量水溶解,再加入稍过量氯化钡溶液,用酚酞作指示剂,用标准浓度的盐酸滴定 |
| C、用分液漏斗分离苯与硝基苯 |
| D、除去氯化铁酸性溶液中的氯化亚铁:加入适量的过氧化氢水溶液 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
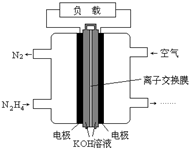 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述不正确的是( )
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述不正确的是( )| A、电流从右侧电极经过负载后流向左侧电极 |
| B、负极发生的电极反应式为N2H4+4OH--4e-═N2+4H2O |
| C、该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
| D、该燃料电池持续放电时,K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
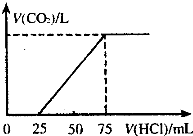 有10mL NaOH溶液,向其中通入一定量的CO2,得到了Na2CO3和NaHCO3的混合溶液.向所得溶液中逐滴加入0.1mol/L的盐酸,边加边振荡.使其充分反应,产生CO2气体的体积(标准状况)与所加盐酸体积之间的关系如图所示.
有10mL NaOH溶液,向其中通入一定量的CO2,得到了Na2CO3和NaHCO3的混合溶液.向所得溶液中逐滴加入0.1mol/L的盐酸,边加边振荡.使其充分反应,产生CO2气体的体积(标准状况)与所加盐酸体积之间的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| 溴 | 物理性质 | 暗红色液体,剌激性气味.室温下易挥发.熔点-7.2℃,沸点59.1℃.密度2.928g?cm-3.稍溶于冷水. |
| 化学性质 | 溶于水生成次溴酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 平衡浓度/(mol L-1) | |
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | 0.1 | |
| 成分 | 含量/(mg L-1) | 成分 | 含量/(mg L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Br- | 64 |
| Mg2+ | 1272 |
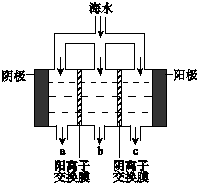 电渗析法淡化海水示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.
电渗析法淡化海水示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA | ||
B、常温常压下,1g氧气含O2分子数目为
| ||
| C、1mol Na2O2晶体中含阴、阳离子总数为4NA | ||
| D、高温高压下合成1mol NH3,要断裂的H-H键数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的碱 |
| B、相同温度下,等物质的量浓度的Na2CO3和NaHCO3溶液pH:Na2CO3>NaHCO3 |
| C、将两支蘸有浓盐酸和浓氨水的玻璃棒相互靠近有大量白烟产生 |
| D、HCl、NH3、CO2都极易溶于水,都可用水作吸收剂做喷泉实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | A | B | C | D |
| 正反应速率/(mol?L-1?min-1) | υ (W)=1.0 | υ (W)=2.0 | υ (X)=1.0 | υ (X)=1.0 |
| 逆反应速率/(mol?L-1?min-1) | υ (Y)=1.0 | υ (X)=3.0 | υ (Y)=1.0 | υ (Z)=1.5 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验目的 | 实验设计 |
| A | 证明盐酸酸性比醋酸强 | 用同一电路测等体积盐酸、醋酸溶液的导电性 |
| B | 证明H2CO3酸性比H2SiO3强 | 将CO2通入Na2SiO3溶液中 |
| C | 证明钠的金属活动性比铜强 | 向CuCl2溶液中投入金属钠 |
| D | 证明溶液中含有I- | 往溶液中加入淀粉 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com