
 CH3OH(g)+H2O(g)���������������������£��¶ȶԷ�Ӧ��Ӱ�죬��ͼ��ʾ��ע��T1��T2������300�棩������˵����ȷ����
CH3OH(g)+H2O(g)���������������������£��¶ȶԷ�Ӧ��Ӱ�죬��ͼ��ʾ��ע��T1��T2������300�棩������˵����ȷ����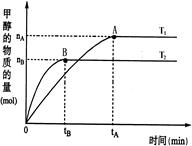
A���¶�ΪT1ʱ���ӷ�Ӧ��ʼ��ƽ�⣬���ɼ״���ƽ������Ϊ��v(CH3OH)=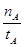 mol��L-1��min-1 mol��L-1��min-1 |
| B��T1> T2 |
| C���÷�ӦΪ���ȷ�Ӧ |
D���¶�ΪT2ʱ�������������СΪ1L���״���ƽ��Ũ��Ϊ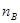 mol��L-1 mol��L-1 |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z3(g) �ﵽ��ѧƽ��״̬��ȡ���д�ʩƽ�ⲻ�ᷢ���ƶ�����
2Z3(g) �ﵽ��ѧƽ��״̬��ȡ���д�ʩƽ�ⲻ�ᷢ���ƶ�����| A������X2 | B����С��������� | C�������¶� | D��ʹ�ô��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NO2 (g)�����н��۲���˵��������Ӧ�ڸ��������Ѿ��ﵽƽ��״̬����
2NO2 (g)�����н��۲���˵��������Ӧ�ڸ��������Ѿ��ﵽƽ��״̬����| A���ڢۢޢ� | B���٢ܢ� | C��ֻ�Т٢� | D��ֻ�Тߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
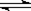 4 C��g�� 2minʱ��Ӧ�ﵽƽ��״̬���¶Ȳ��䣩�������C ��Ũ��Ϊ0.4 mol/L������д���пհף�
4 C��g�� 2minʱ��Ӧ�ﵽƽ��״̬���¶Ȳ��䣩�������C ��Ũ��Ϊ0.4 mol/L������д���пհף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z��g������H<0(����ӦΪ���ȷ�Ӧ)���ڲ�ͬ�¶ȣ�T1��T2����ѹǿ��P1��P2���£�����Z�����ʵ���[n��Z��]�뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ���������ж���ȷ����
2Z��g������H<0(����ӦΪ���ȷ�Ӧ)���ڲ�ͬ�¶ȣ�T1��T2����ѹǿ��P1��P2���£�����Z�����ʵ���[n��Z��]�뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ���������ж���ȷ����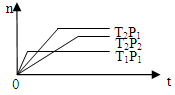
| A��T1<T2��P1<P2 | B��T1<T2��P1>P2 | C��T1>T2��P1>P2 | D��T1>T2��P1<P2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 4C��g��+D��g����Ӧ10min���ƽ�⣬��ʱD��Ũ��Ϊ0.5mol/L������˵����ȷ����
4C��g��+D��g����Ӧ10min���ƽ�⣬��ʱD��Ũ��Ϊ0.5mol/L������˵����ȷ����  A��ת����һ������50%
A��ת����һ������50%�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com