
500℃条件下,在恒容密闭容器中,充入1molNO2存在如下平衡2NO2(g) N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的
N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的
A.平衡向正反应方向移动 B.平衡常数K增大
C.NO2的转化率变小 D.容器内气体颜色先变深后变浅,最后比原来还要浅
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
在元素周期表中,元素A、B位于同周期,A在ⅡA族,B在ⅢA族。A的原子序数为a, B的原子序数为b,不可能是
A.b=a+1 B.b=a+11 C.b=a+10 D.b=a+25
查看答案和解析>>
科目:高中化学 来源: 题型:
 下列离子方程式正确的是
下列离子方程式正确的是

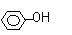 A.用惰性电极电解饱和食盐水:2Cl-+2H2O Cl2↑+H2↑+2OH-
A.用惰性电极电解饱和食盐水:2Cl-+2H2O Cl2↑+H2↑+2OH-
B.苯酚与碳酸钠溶液: + CO32—→ + H2CO3
C.等体积等物质的量浓度的NH4Fe(SO4)2和Ba(OH)2混合:
2Fe3++ 3SO42-+ 3Ba2++6OH-→3BaSO4↓+ 2Fe(OH)3↓
D.在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:
3ClO-+2Fe(OH)3→2FeO42-+3Cl-+ H2O+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:

48.写出反应Ⅰ的反应试剂和反应条件 。
49.写出反应类型。反应Ⅱ 反应Ⅲ 。
50.写出结构简式。E F 。
51.写出G→M的化学反应方程式 。
52.反应Ⅰ能否省略? ;说明原因 。
53.从E→F经过两步,这两步的次序能否颠倒? ;说明原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,书写正确的是
A.弱酸酸式盐NaHB在水溶液中水解:HB–+H2O H3O++B2–
H3O++B2–
B.电解饱和食盐水:C1-+2H2O H2↑+Cl2↑+OH-
H2↑+Cl2↑+OH-
C.氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e一=4OH-
D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用0.10 mol/L标准NaOH溶液滴定某浓度的盐酸。记录数据如下:
| 实验序号 | 待测液体积(mL) | 所消耗NaOH标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.54 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.36 |

(1)滴定时选用酚酞试液作指示剂,如何判断滴定达到终点 。
(2)盐酸的物质的量浓度为_____________
(3)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是 (填“偏高”或“偏低”或“无影响”,下同)。
(4)某同学用已知准确浓度的高锰酸钾溶液滴定溶液中Fe2+的浓度,高锰酸钾溶液应盛放在 中(填“甲”或“乙”),该反应的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.从海水中提取物质都必须通过化学反应才能实现
B.将盛满二氧化氮气体的试管倒立在水中,可观察到溶液充满试管
C.金属镁着火可用CO2灭火
D.向 FeSO4溶液中滴加NaOH溶液,先出现白色沉淀,最终沉淀转化成红褐色
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氨气和氯气混合可发生下列反应: 2NH3+3Cl2 → 6HCl+N2,NH3+HCl → NH4Cl。
常温常压下,取总物质的量为12mol的氯气和氨气的混合气体,完全反应后,气体总物质的量保持不变。做54、55题
反应前氯气和氨气的物质的量之比为______________ (要求解题过程)
反应后生成的氧化产物的质量为_________________(要求解题过程)
某天然碱(纯净物)可看作由CO2和NaOH反应后的产物所组成。称取天然碱样品四份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30mL,产生CO2的体积(标准状况)如下表:
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
| 盐酸液的体积(mL) | 30 | 30 | 30 | 30 |
| 样品(g) | 3.32 | 4.15 | 5.81 | 7.47 |
| 二氧化碳的体积(mL) | 672 | 840 | 896 | 672 |
由第Ⅰ组数据中的CO2体积与样品质量之比,可以推测用2.49g样品进行同样的实验时,产生CO2_________mL(标准状况)。(要求解题过程)
另取3.32g天然碱样品于300℃加热分解至完全(300℃时NaCO3不分解),产生CO2112mL(标准状况)和水0.45g,计算并确定该天然碱的化学式(要求解题过程)。
由上表中第Ⅳ组数据可以确定所用的HCl(aq)的浓度为 _______2.5
mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com