
下列有关有机物性质的说法正确的是( )
A.蛋白质可以与酸、碱或重金属盐反应
B.芳香烃都不能使酸性KMnO4溶液褪色
C.CH3CH2OH与氢溴酸能反应
D.石油的分馏可获得乙烯、丙烯等不饱和烃
科目:高中化学 来源: 题型:
用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为

面心立方最密堆积(如右图),已知该晶体的密度为9.00 g·cm-3,晶胞中该原子的配位数为________;Cu的原子半径为________cm(阿伏加德罗常数为NA,要求列式计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)质子数为35、中子数为45的溴原子: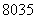 Br( )
Br( )
(2014·江苏,2B)
(2)硫离子的结构示意图: ( )
( )
(2014·江苏,2C)
(3)核外电子排布相同的微粒化学性质也相同( )
(2014·山东理综,8B)
(4)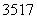 Cl与
Cl与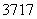 Cl得电子能力相同( )
Cl得电子能力相同( )
(2014·山东理综,8D)
(5)氯原子的结构示意图: ( )
( )
(2013·江苏,2C)
(6)中子数为146、质子数为92的铀(U)原子: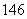 92U( )
92U( )
(2013·江苏,2D)
(7)原子核内有18个中子的氯原子: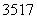 Cl( )
Cl( )
(2012·海南,9D)
(8)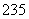 92U和
92U和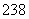 92U是中子数不同质子数相同的同种核素( )
92U是中子数不同质子数相同的同种核素( )
(2012·天津理综,3C)

(9)元素周期表中铋元素的数据见右图,则:
①Bi元素的质量数是209( )
②Bi元素的相对原子质量是209.0( )
(2012·上海,6改编)
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G、L、I九种主族元素分别位于三个不同的短周期,它们的原子序数依次增大,其中B、C、D位于同一周期,A与E、B与G、D与L分别位于同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F最外层电子数的2倍,C和D的最外层电子数之和为11。请回答下列问题:
(1)以上元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)__________________________,E、F、L所形成的简单离子的半径由大到小的顺序为(用离子符号表示)____________。
(2)L、I两元素可按原子个数比1∶1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为__________________________________________。
(3)固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生,写出该反应的离子方程式:_______________________。
(4)由A、B、C、D按原子个数比4∶1∶1∶2形成一种化合物Y,则Y的化学式为________________________,向Y中加足量稀硫酸后,再加高锰酸钾溶液,高锰酸钾溶液褪色。写出使高锰酸钾溶液褪色的反应的离子方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活密切相关,下列说法正确的是( )
A.蛋白质和油脂都是天然高分子化合物
B.CO2和CH4都是造成温室效应的气体
C.蔗糖和麦芽糖的水解产物均为葡萄糖
D.苯酚和甲苯遇FeCl3均显紫色
查看答案和解析>>
科目:高中化学 来源: 题型:
在1 L K2SO4和CuSO4的混合溶液中c(SO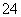 )=2.0 mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )
)=2.0 mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )
A.2.0 mol·L-1 B.1.5 mol·L-1
C.1.0 mol·L-1 D.0.50 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数,在含4 g NaOH溶质的溶液中通入一定量的CO2,将溶液蒸干并灼烧,最后得到的固体可能是( )
A.0.1NA的NaHCO3
B.0.05NA Na2CO3
C.0.05NA~0.1NA Na2CO3和NaHCO3混合物
D.0.1NA的NaHCO3和NaOH混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化。
(1)该同学最初的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅰ | 先向2 mL 0.1 mol·L-1 FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | |
| Ⅱ | 先向2 mL 0.1 mol·L-1 FeCl3溶液中滴加KSCN溶液,再滴加0.1 mol·L-1 KI溶液 | 滴加KSCN溶液后,溶液变成血红色;滴加KI溶液后,血红色无明显变化 |
①实验Ⅰ的现象为________________________________________________。
②FeCl2溶液与新制氯水反应的离子方程式为____________________________
________________________________________________________________________。
(2)该同学分析了导致实验Ⅱ现象的可能原因,并对实验方案进行了改进。改进后的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅲ | 向2 mL 0.1 mol·L-1 KI溶液中滴加1 mL | |
| 0.1 mol·L-1 FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成血红色 |
根据实验Ⅲ,该同学认为Fe3+有可能与I-发生氧化还原反应,请结合实验现象用简明的文字说明他得出上述结论的理由:_____________________________________________。
(3)该同学认为需要进一步设计实验,证明根据实验Ⅲ中现象得出的结论。请补全下表中的实验方案:
| 编号 | 操作 | 预期现象及结论 |
| Ⅳ | 向2 mL 0.1 mol·L-1 KI溶液中滴加1 mL 0.1 mol·L-1 FeCl3溶液,__________ |
(4)上述实验结果表明,Fe3+有可能与I-发生氧化还原反应。进一步查阅资料知,参加反应的Fe3+与I-的物质的量相同。该同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变血红的原因,认为Fe3+与I-反应的离子方程式应写为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是( )
A.由Al、Cu、稀H2SO4组成的原电池,负极反应式为Al-3e-===Al3+
B.由Mg、Al、NaOH溶液组成的原电池,负极反应式为Al-3e-+4OH-===AlO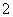 +2H2O
+2H2O
C.由Fe、Cu、FeCl3溶液组成的原电池,负极反应式为Cu-2e-===Cu2+
D.由Al、Cu、浓硝酸组成的原电池,负极反应式为Cu-2e-===Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com