
| A. | ①②③④⑤ | B. | ①②④⑤ | C. | ①②③④ | D. | ②④⑤ |
分析 比较非金属性可通过以下角度:氢化物的稳定性;与氢气反应的难易程度;最高价氧化物对应的水化物的酸性;单质之间的置换反应;对应阴离子的还原性强弱;与变价金属反应的化合价高低等.
解答 解:①元素的非金属性越强,对应的氢化物越稳定,HCl比H2S稳定,Cl比一S非金属性强,故①正确;
②元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,HClO4酸性比H2SO4强,Cl比S非金属性强,故②正确;
③元素的非金属性越强,对应的单质的氧化性越强,Cl2能与H2S反应生成S,Cl比S非金属性强,故③正确;
④Cl2比S更易与H2化合生成相应气态氢化物,说明Cl比S非金属性强,故④正确;
⑤比较元素的非金属性应用元素对应最高价氧化物的水化物的酸性强弱比较,不能根据氢化物的酸性强弱比较,例如HF溶液的酸性比HCl弱,但非金属性:F>Cl,不能说明非金属性的强弱,故⑤错误;
故选C.
点评 本题考查非金属性的比较,学习中注意把握比较非金属性强弱的角度,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
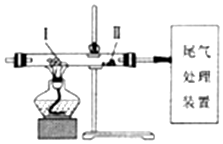
| A. | 缓慢通入N2,再加热Ⅰ处的碳酸氢钠,可观察到Ⅱ处过氧化钠粉末由浅黄色变成白色 | |
| B. | 缓慢通入N2,加热Ⅰ处KClO3和MnO2的混合物,可观察到Ⅱ处干燥KI淀粉试纸变成蓝色 | |
| C. | 先对Ⅰ处的氯化铵加热,再缓慢通入N2,可看到Ⅰ处固体减少,Ⅱ处无固体沉积 | |
| D. | 先缓慢通入CO2,再加热Ⅰ处炭粉,可观察到Ⅱ处氧化铁粉末由红色变成黑色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水鉴别乙烯和CO2 | |
| B. | 用pH试纸鉴别NaCl溶液与Na2CO3溶液 | |
| C. | 用观察外观颜色的方法区别氧化铁和氧化铜 | |
| D. | 用石灰水鉴别CO2和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂和蛋白质均是高分子化合物 | |
| B. | 雾能产生丁达尔效应,雾属于胶体 | |
| C. | 新制氯水、HClO和SO2都有漂白作用 | |
| D. | 硝酸能与苯发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该物质为有机物 | B. | 该物质为无机物 | ||
| C. | 该物质由三种元素组成 | D. | 该物质燃烧产物可能含CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L溶液中含1 mol硫酸根离子的H2SO4溶液 | |
| B. | 将500克胆矾溶于2升水中 | |
| C. | 200mL溶液中含32克硫酸铜的溶液 | |
| D. | 把125克胆矾溶于水,配成500mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
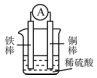
| A. | 铜棒逐渐溶解,溶液由无色慢慢地变为黄色 | |
| B. | 铁棒为负极,电子从铁棒经外电路流向铜棒 | |
| C. | 电池工作一段时间后,溶液的酸性将增强 | |
| D. | 该电池的总反应为Fe2++Cu═Fe+Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com