
分析 该燃料电池中,正极上氧气得电子和二氧化碳反应生成碳酸根离子,在得失电子相同条件下将正负极电极反应式相加即可得电池反应式,据此分析解答.
解答 解:该熔融盐燃料电池中,正极上氧气得电子和二氧化碳反应生成碳酸根离子,电极反应式为O2+2CO2+4e-═2CO32-,又负极电极反应式为2CO+2CO32--4e-═4CO2,在得失电子相同条件下将正负极电极反应式相加得电池反应式2CO+O2═2CO2,
故答案为:O2+2CO2+4e-═2CO32-;2CO+O2═2CO2.
点评 本题考查化学电源新型电池,侧重考查电极反应式的书写,燃料电池电极反应式的书写是学习难点,燃料电池中,负极上燃料失电子、正极上氧化剂得电子,题目难度中等.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:解答题
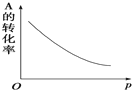 密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡状态,经测定增大压强p时,A的转化率随p而变化的曲线如图所示:
密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡状态,经测定增大压强p时,A的转化率随p而变化的曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴水褪色与苯使溴水褪色的原因相同 | |
| B. | 欲将蛋白质从溶液中析出而又不改变它的性质,可加CuSO4溶液 | |
| C. | 用大米酿造的酒在一定条件下密封保存,时间越长越香醇 | |
| D. | 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com