
| A. | 常温下,1mol•L-1的Na2CO3溶液中CO32-的数目小于NA | |
| B. | 常温常压下,1.7g NH3中所含的原子数为0.4NA | |
| C. | 向含0.1mol NH4Al(SO4)2的溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目为0.4NA | |
| D. | 标准状况下,4.48LNO2与足量的水反应,转移的电子数为0.1NA |
分析 A.溶液体积未知;
B.质量转化为物质的量,结合1个氨气分子含有4个原子解答;
C.含0.1mol NH4Al(SO4)2的溶液中滴加NaOH,消耗的OH-数目为0.4NA时反应生成氢氧化铝、一水合氨和硫酸钠;
D.二氧化氮与水反应生成硝酸和一氧化氮,二氧化氮既做氧化剂又做还原剂.
解答 解:A.溶液体积未知,只知道浓度无法计算微粒个数,故A错误;
B.常温常压下,1.7g NH3物质的量为$\frac{1.7g}{17g/mol}$=0.1mol,含有原子物质的量为0.4mol,所含的原子数为0.4NA,故B正确;
C.含0.1mol NH4Al(SO4)2的溶液中滴加NaOH,消耗的OH-数目为0.4NA时反应生成氢氧化铝、一水合氨和硫酸钠,此时沉淀未溶解,故C错误;
D.二氧化氮与水反应生成硝酸和一氧化氮,方程式:3NO2+H2O═2HNO3+NO,消耗3mol二氧化氮,转移2mol电子,则标准状况下,4.48LNO2物质的量为0.2mol,与足量的水反应,转移的电子数为$\frac{0.4}{3}$NA,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意二氧化氮与水发生歧化反应,题目难度中等.


科目:高中化学 来源: 题型:多选题
| A. | CuO作还原剂 | B. | 铜元素化合价降低 | ||
| C. | CuO作氧化剂 | D. | 铜元素化合价升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a+b<c+d,则反应一定能自发向右进行 | |
| B. | 若起始时A、B的物质的量之比为a:b,则平衡时的转化率之比为1:1 | |
| C. | 若a+b=c+d,在平衡体系中共有气体m mol,再向其中充入n molB,则平衡时气体的总物质的量小于(m+n)mol | |
| D. | 若a+b=c,则对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
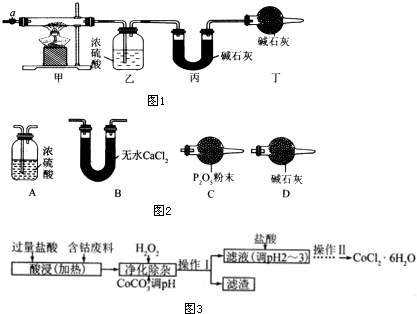
| 乙装置的质量/g | 丙装置的质量/g | |
| 加热前 | 80.00 | 62.00 |
| 加热后 | 80.36 | 62.88 |
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
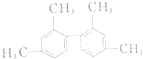
| A. | 等质量的该烃和甲烷均完全燃烧,耗氧量后者小于前者 | |
| B. | 该烃能使酸性高锰酸钾溶液褪色,属于苯的同系物 | |
| C. | 分子中一定有11个碳原子处于同一平面上 | |
| D. | 该烃的一氯取代产物为6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
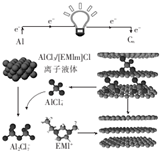 英国《自然》杂质近期报道了一种用泡沫石墨烯(CW)作为正极材料的新型铝离子电池,其放电时的工作原理如图所示,下列说法不正确的是( )
英国《自然》杂质近期报道了一种用泡沫石墨烯(CW)作为正极材料的新型铝离子电池,其放电时的工作原理如图所示,下列说法不正确的是( )| A. | 放电时,若外电路中转移1mol电子,则负极质量减少9g | |
| B. | 充电时,石墨烯作阳极 | |
| C. | 充电时,阴极的电极反应式为AlCl4-+3e-═Al+4Cl- | |
| D. | 放电时,正极的电极反应式为CW(AlCl4)+e-═CW+AlCl4- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H3PO4 | D. | 熔点:NaCl>Na>CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com