
 ���շۣ�Na2S2O4����ǿ��ԭ�ԣ��ڿ������ױ����������ڼ��Ի����½��ȶ���ijʵ��С��������ͼװ����ȡ���շۣ��г�װ����ʡ�ԣ�
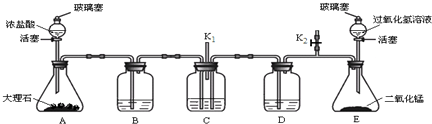
���շۣ�Na2S2O4����ǿ��ԭ�ԣ��ڿ������ױ����������ڼ��Ի����½��ȶ���ijʵ��С��������ͼװ����ȡ���շۣ��г�װ����ʡ�ԣ����� ��1�����շۣ�Na2S2O4����ǿ��ԭ�ԣ��ڿ������ױ���������������ȡ���շ�ʱ��װ���в����п�����
��2����������������ˮ������̼�����Ʒ�Ӧ���ɶ�����̼����������Ũ���ᣬ��������������Һ���ܽ�Ⱥ�С��
��3��δ��Ӧ�Ķ����������Ⱦ����������Ҫ���գ�ͬʱ��������������ˮ��������������ݴ˴��⣻
��4����SO2��HCOONa��NaOH��Ӧ������Na2S2O4��ͬʱ����CO2���壬����Ԫ���غ��д��ѧ����ʽ��
�ڸ����ṩ���Լ����鷴Ӧ�Ļ������CO2�������ȳ�ȥ�����е�δ��Ӧ�Ķ���������ͨ������ʯ��ˮ���飻
��5��Na2S2O4����ǿ��ԭ�ԣ����Ա�������������������ӣ�ͨ��������������ӿ��ж��䱻������
��6�����շۣ�Na2S2O4���������ڳ�ȥ���Է�ˮ�е�Cr2O72-�����շ۱�����Ϊ������Cr2O72-ת��ΪCr3+�����ݵ��ӵ�ʧ�غ��й�ϵʽNa2S2O4��Cr2O72-������Cr2O72-�����ʵ������㱣�շ۵�������
��� �⣺��1�����շۣ�Na2S2O4����ǿ��ԭ�ԣ��ڿ������ױ���������������ȡ���շ�ʱ��װ���в����п���������ʵ��ǰ��ͨһ��ʱ���N2��Ŀ�����ž�װ���ڵ�������
�ʴ�Ϊ���ž�װ���ڵ�������
��2����������������ˮ������̼�����Ʒ�Ӧ���ɶ�����̼����������Ũ���ᣬ��������������Һ���ܽ�Ⱥ�С��
��ѡbd��
��3��δ��Ӧ�Ķ����������Ⱦ����������Ҫ���գ�ͬʱ��������������ˮ�����������������װ��D�����������ն�������β������ֹ��Ⱦ������ͬʱ��������
�ʴ�Ϊ�����ն�������β������ֹ��Ⱦ������ͬʱ��������
��4����SO2��HCOONa��NaOH��Ӧ������Na2S2O4��ͬʱ����CO2���壬��Ӧ�Ļ�ѧ����ʽΪHCOONa+NaOH+2SO2=Na2S2O4+CO2+H2O��
�ʴ�Ϊ��HCOONa+NaOH+2SO2=Na2S2O4+CO2+H2O��
�ڸ����ṩ���Լ����鷴Ӧ�Ļ������CO2��Ҫ�ȳ�ȥ�����е�δ��Ӧ�Ķ�������Ҫ��ͨ�����������Һ����ͨ��Ʒ�������������Ƿ��������ͨ������ʯ��ˮ���飬֤���ж�����̼������ΪƷ����Һ����ɫ������ʯ��ˮ��룬
�ʴ�Ϊ��c��a��Ʒ����Һ����ɫ������ʯ��ˮ��룻
��5��Na2S2O4����ǿ��ԭ�ԣ����Ա�������������������ӣ�ͨ��������������ӿ��ж��䱻������������֤Na2S2O4����ǿ��ԭ�ԣ�ѡ�õ�����Լ�ΪH2O2��Һ��BaCl2��Һ��
��ѡc��
��6�����շۣ�Na2S2O4���������ڳ�ȥ���Է�ˮ�е�Cr2O72-�����շ۱�����Ϊ������Cr2O72-ת��ΪCr3+�����ݵ��ӵ�ʧ�غ��й�ϵʽNa2S2O4��Cr2O72-��0.01mol•L-1��100mL���Է�ˮ�е�Cr2O72-�����ʵ���Ϊ0.001mol�����Ա��շ۵�����Ϊ0.001mol��174g/mol=0.174g��
�ʴ�Ϊ��0.174��
���� ������Ҫ����ѧ������Ŀ�л�ȡ��Ϣ�������Լ����ݻ�õ���Ϣ�����ѧ��ѧ֪ʶ����������������Ŀ���õ��Ļ�ѧ֪ʶ�и��ݵ��ӵ�ʧ�غ�������غ㶨�ɽ�����ؼ��㡢ʵ���������������֪ʶ���ۺ���ǿ�����Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
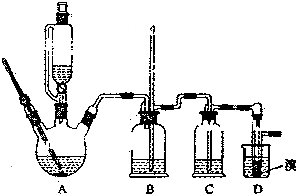 ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�
ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm3 | 0.79 | 2.2 | 0.71 |
| �е�/��C | 78.5 | 132 | 34.6 |
| �۵�/��C | -130 | 9 | -116 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ������� | ��ʼʱ���������ʵ���/mol | �ﵽƽ��ʱ��ϵ�����ı仯 | ||
| A | B | C | ||
| �� | 2 | 1 | 0 | 0.75Q kJ |
| �� | 0.4 | 0.2 | 1.6 | |
| A�� | �����١����з�Ӧ��ƽ�ⳣ����Ϊ4 | |
| B�� | �������дﵽƽ��ʱ�ų�������Ϊ0.05QkJ | |
| C�� | ����������ͨ�뺤����ƽ��ʱA��ת���ʲ��� | |
| D�� | �����������䣬�������ڱ��ֺ��ݾ��ȣ���ﵽƽ��ʱC���������С��$\frac{2}{3}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ı���������������һ�ָ���Ч�Ĵ�������Ӧ���ȵ�ʱ������� | |
| B�� | ��ƽ�����������ֻ����O2������߷�Ӧ���� | |
| C�� | �ﵽƽ��ʱ��SO2��ת������80% | |
| D�� | ��ƽ��������ͨ�����BaCl2��Һ�У��õ�����������Ϊ114.90g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʯ���ڴ�����Һ��CaCO3+2H+�TCa2++CO2��+H2O | |
| B�� | ��FeBr2��Һ��ͨ������������2Fe2++4Br++3Cl2�T2Fe3++2Br2+6Cl- | |
| C�� | NH4HCO3���ڹ�����NaOH��Һ�У�HCO3-+OH-�TCO32-+H2O | |
| D�� | ��������KAl��SO4��2•12H2O��Һ�еμ�Ba��OH��2��Һ��ǡ��ʹSO42-������ȫ��2Al3++3SO42-+3Ba2++6OH-�T2Al��OH��3��+3BaSO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��Fe��=0.5 mol/��L•min�� | B�� | v��H2SO4��=1 mol/��L•min�� | ||
| C�� | v��H2SO4��=0.5 mol/��L•min�� | D�� | v��FeSO4��=1 mol/��L•min�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com