
【题目】下列反应不属于氧化还原反应的是
A. Zn+2HCl===ZnCl2+H2↑
B. Ca(ClO)2+2HCl===CaCl2+2HClO
C. Pb3O4+8HCl(浓)===3PbCl2+Cl2↑+4H2O
D. 3Cl2+6KOH(浓)![]() 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O
【答案】B
【解析】
反应过程中不存在电子转移,说明不是氧化还原反应,据此判断。
A. 反应Zn+2HCl=ZnCl2+H2↑中锌失去电子,氢元素得到电子,是氧化还原反应,存在电子转移,A不符合;
B. 反应Ca(ClO)2+2HCl=CaCl2+2HClO中元素的化合价均没有发生变化,不是氧化还原反应,不存在电子转移,B符合;
C. 反应Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O中氯元素失去电子,铅元素得到电子,是氧化还原反应,存在电子转移,C不符合;
D. 反应3Cl2+6KOH(浓)![]() 5KCl+KClO3+3H2O中氯元素化合价部分升高部分降低,属于氧化还原反应,存在电子转移,D不符合。
5KCl+KClO3+3H2O中氯元素化合价部分升高部分降低,属于氧化还原反应,存在电子转移,D不符合。
答案选B。


科目:高中化学 来源: 题型:
【题目】已知Cu2O能与稀硝酸反应:Cu2O+HNO3→Cu(NO3)2+NO↑+H2O(未配平),若生成的NO在标况下的体积为0.448L,下列说法正确的是
A. 转移的电子总数为0.06NA
B. 作氧化剂的HNO3是0.14mol
C. 至少需要0.5mo/L的硝酸140mL与Cu2O反应
D. 被氧化的Cu2O是144g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为Fe2O3和CuO的混合物且氧化性强弱顺序:Fe3+>Cu2+>H+>Fe2+。X样品可发生如图所示的转化关系:
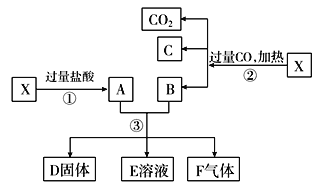
(1)写出步骤③可能发生反应的离子方程式:________________________(共有3个,任写一个即可)。
(2)若溶液E中只有一种金属离子,则一定是__________;若溶液E中含有两种金属离子,则一定是________。
(3)若D固体是纯净物,该固体是________(填化学式)。
(4)印刷电路板是由高分子材料和铜箔复合而成的,可用FeCl3溶液作“腐蚀剂”刻制印刷电路板,该过程发生反应的离子方程式为____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在镁屑和无水乙醚的混合体系中,滴加卤代烷,反应后得到的有机镁化合物称为格氏试剂。制备的格氏试剂不需要分离就可直接用于有机合成,是重要的有机合成中间体。反应原理为:![]()
利用A(![]() )来合成
)来合成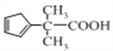 的流程如图所示:
的流程如图所示:

(1)物质A的名称为________;
(2)A![]() B的反应类型是_________;
B的反应类型是_________;
(3)写出由F生成G、G生成H的化学方程式:_____________________________;
(4)D的同分异构体中含有六元环且能发生银镜反应的有___________种;
(5)写出符合下列要求的I的同分异构体的结构简式_________;(写一种即可,已知同一个碳原子上不能连接2个羟基)
①芳香族化合物 ②二元醇 ③分子中有5种不同化学环境的H原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应,若生成硫酸钡沉淀的质量比为1∶2∶3,则三种硫酸盐的物质的量浓度之比为( )
A. 1∶2∶3 B. 1∶6∶9 C. 1∶3∶3 D. 1∶3∶6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象的记录不正确的是( )
A.钠可以在氯气中燃烧,产生白色的烟
B.红热的铜丝可以在氯气中燃烧,生成红棕色的烟
C.纯净的氢气可以在氯气中安静燃烧,发出苍白色火焰
D.氯气作用于干燥的品红试纸,试纸不褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铅蓄电池电解甲、乙电解池中的溶液。己知铅蓄电池的总反应为:Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(l)电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( )
2PbSO4(s)+2H2O(l)电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( )

A. d极为阴极
B. 放电时铅蓄电池负极的电极反应式为:PbO2(s)+4H+(aq)+SO42-(aq)+4e-=PbSO4(s)+2H2O(l)
C. 若利用甲池精炼铜,b极应为粗铜
D. 若四个电极材料均为石墨,当析出6.4gCu时,两池中共产生气体3.36L(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.76 g铜镁合金完全溶解于50 mL、密度为1. 40 g cm-3、质量分数为63%的浓硝酸中,得到NO2气体1 792 mL(标准状况),向反应后的溶液中加入适量的1.0 mol L-1的NaOH 溶液,恰使溶液中的金属离子全部沉淀。下列说法不正确的是
A. 该浓硝酸中的HNO3的物质的量浓度是14.0 mol L-1
B. 加入NaOH溶液的体积是50 mL
C. 浓硝酸在与合金的反应中起了酸性和氧化性的双重作用,且起氧化性的硝酸的物质的量为0.08 mol
D. 得到的金属氢氧化物的沉淀为3.12 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com