
【题目】室温下,用0.100 0 mol·L-1NaOH溶液分别滴定体积均为20.00 mL的盐酸和醋酸溶液,滴定曲线如右图。下列说法正确的是
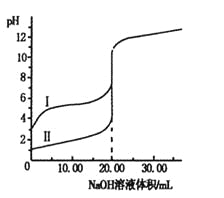
A.I、Ⅱ分别表示盐酸和醋酸的滴定曲线
B.盐酸和醋酸的浓度均为0.100 0 mol·L-1
C.pH=7时,两种酸所消耗NaOH溶液的体积相等
D.V(NaOH)=20.00mL时,c(Cl一)=c(CH3COO一)
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】某化学实验小组欲测定铁的氧化物![]() 样品组成,查阅资料发现:甲酸
样品组成,查阅资料发现:甲酸![]() 是一种有刺激性气味的无色液体,易挥发,有较强的还原性,熔点
是一种有刺激性气味的无色液体,易挥发,有较强的还原性,熔点![]() ,沸点
,沸点![]() ,能与水、乙醇互溶,甲酸与浓硫酸共热可制备一氧化碳:HCOOH
,能与水、乙醇互溶,甲酸与浓硫酸共热可制备一氧化碳:HCOOH![]() H2O+CO↑,制备时先加热浓硫酸至
H2O+CO↑,制备时先加热浓硫酸至![]() ,再逐滴滴入甲酸。根据以上信息设计了实验装置,如图所示:
,再逐滴滴入甲酸。根据以上信息设计了实验装置,如图所示:
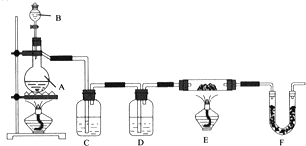
请回答下列问题:
![]() 仪器中装入的试剂:B ______ 、C ______ 、D ______。
仪器中装入的试剂:B ______ 、C ______ 、D ______。
![]() 该实验装置A仪器中须添加一种玻璃仪器,其名称为______;连接好装置后应首先______。
该实验装置A仪器中须添加一种玻璃仪器,其名称为______;连接好装置后应首先______。
![]() “加热反应管E”和“从B向A逐滴滴加液体”这两步操作应该先进行的是______
“加热反应管E”和“从B向A逐滴滴加液体”这两步操作应该先进行的是______![]() 在这两步之间还应进行的操作是______。
在这两步之间还应进行的操作是______。
![]() 反应过程中F管
反应过程中F管![]() 内盛碱石灰
内盛碱石灰![]() 逸出的气体是______,其处理方法是______。
逸出的气体是______,其处理方法是______。
![]() 测得下列数据
测得下列数据![]() 空E管的质量为
空E管的质量为![]() ;
;![]() 管和
管和![]() 样品的总质量为
样品的总质量为![]() ;
;![]() 反应后冷却至室温称量E管和铁粉的总质量为
反应后冷却至室温称量E管和铁粉的总质量为![]() 经确认样品全部变为铁粉
经确认样品全部变为铁粉![]() 计算可知该铁的氧化物化学式为______。
计算可知该铁的氧化物化学式为______。
![]() 设计实验证明:
设计实验证明:
![]() 甲酸的酸性比碳酸的强______。
甲酸的酸性比碳酸的强______。
![]() 的氧化性比
的氧化性比![]() 的弱______。
的弱______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是
A. 用干燥洁净的玻璃棒蘸取![]() 溶液,点到置于表面皿的pH试纸上测pH
溶液,点到置于表面皿的pH试纸上测pH
B. 氢氧化钠固体或碱石灰既可与浓氨水作用制得氨气,也可用于干燥氨气
C. 双氧水不稳定,见光、遇热、遇大多数金属氧化物都会加快它的分解,但在碱性环境下分解较慢
D. 海带中提取碘的过程中,可用过量的氯气或双氧水氧化水溶液中的![]() ,得到碘单质
,得到碘单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系.根据要求回答问题:
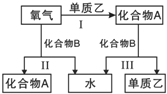
![]() 如图三个反应中,属于氧化还原反应的有______个.
如图三个反应中,属于氧化还原反应的有______个.
![]() 若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有______.
若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有______.
A.还原性:![]() B.酸性:
B.酸性:![]()
C.稳定性:![]() C.沸点:
C.沸点:![]()
![]() 若化合物B常温下为气体,其水溶液呈碱性
若化合物B常温下为气体,其水溶液呈碱性![]() 答题必须用具体物质表示
答题必须用具体物质表示![]() .
.
![]() 化合物B的电子式为______;其水溶液呈碱性的原因是______
化合物B的电子式为______;其水溶液呈碱性的原因是______![]() 用离子方程式表示
用离子方程式表示![]() .
.
![]() 化合物B可与
化合物B可与![]() 组成燃料电池
组成燃料电池![]() 氢氧化钾溶液为电解质溶液
氢氧化钾溶液为电解质溶液![]() ,其反应产物与反应Ⅲ相同.写出该电池负极的电极反应式______.
,其反应产物与反应Ⅲ相同.写出该电池负极的电极反应式______.
![]() 当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为
当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为![]() 和
和![]() ,则反应Ⅰ的热化学方程式为______
,则反应Ⅰ的热化学方程式为______![]() 注:反应条件相同、所有物质均为气体
注:反应条件相同、所有物质均为气体![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,不溶于水,易溶于醇等有机溶剂。实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
已知:①乙醇在浓硫酸存在下在140℃脱水生成乙醚
2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
②实验中常因温度过高而使乙醇和浓硫酸反应生成少量SO2和CO2,用12.0g溴和足量的乙醇制备1,2-二溴乙烷,实验装置如图所示:
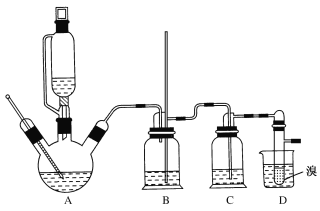
有关数据列表如下:
类别 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是___。要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是___。
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是____。
(3)在装置C中应加入NaOH溶液,其目的是____。
(4)装置D中小试管内盛有液溴,判断该制备反应已经结束的最简单方法是___。
(5)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___层(填“上”或“下”)。若产物中有少量未反应的Br2,最好用___洗涤除去;若产物中有少量副产物乙醚,可用____(填操作方法名称)的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是___。
(7)若实验结束后得到9.4g产品,1,2—二溴乙烷的产率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 38.4g 铜与适量浓硝酸恰好反应生成氮的氧化物,这些氧化物恰好溶解在NaOH溶液中得到NaNO3和NaNO2的混合溶液,反应过程及有关数据如下图所示:

下列有关判断正确的是( )
A. 若浓硝酸体积为 200mL,则其物质的量浓度为 11mol/L
B. NO、NO2、N2O4 和 NaOH 溶液反应时, NO2、N2O4 仅作还原剂
C. 生成 0.2 mol NaNO3 和 0.8 mol NaNO2
D. 硝酸在反应中仅体现氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的铁与一定量的浓HNO3在加热条件下恰好完全反应,得到硝酸铁溶液和NO2 、N2O4 、NO的混合气体,这些气体与6.72 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铁溶液中加入2 mol·L-1 的NaOH 溶液至Fe3+恰好沉淀,则消耗NaOH 溶液的体积是( )
A. 600 mLB. 300 mLC. 240 mLD. 180 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质转化在给定条件下能实现的是( )
①Al2O3![]() NaAlO2(aq)
NaAlO2(aq) ![]() Al(OH)3
Al(OH)3
②S![]() SO3
SO3![]() H2SO4
H2SO4
③NaOH(aq) ![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
④Fe![]() FeCl2
FeCl2![]() FeCl3
FeCl3
A.①③
B.②③
C.②④
D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与纯水的电离相似,液氨中也存在着微弱的电离:2NH3![]() NH4++NH2-,据此判断,以下叙述错误的是( )
NH4++NH2-,据此判断,以下叙述错误的是( )
A.一定温度下液氨中c(NH4+)·c(NH2-)是一个常数
B.液氨中含有NH3、NH4+、NH2-等粒子
C.只要不加入其他物质,液氨中c(NH4+)=c(NH2-)
D.液氨达到电离平衡时c(NH3)=c(NH4+)=c(NH2-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com