
| A£®Ęū³µÅŷŵēóĮæĪ²Ęų |
| B£®Éś²śĮņĖį¹¤³§ÅŷŵÄĪ²Ęų |
| C£®¹¤ŅµÉĻ“óĮæŗ¬ĮņČ¼ĮĻµÄČ¼ÉÕ |
| D£®ĀŅæ³ĄÄ·„£¬ĘĘ»µĮĖÉśĢ¬Ę½ŗā |
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
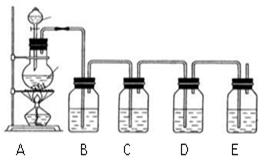
| A£®Ę·ŗģČÜŅŗ | B£®ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ |
| C£®³ĪĒåŹÆ»ŅĖ® | D£®ĒāŃõ»ÆÄĘČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 |
| A£®2SO2+O22SO3 | B£®SO2+H2O H2SO3 H2SO3 |
| C£®SO2+2H2S====3S”ż+2H2O | D£®SO2+Cl2+2H2O====H2SO4+2HCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗ¼ĘĖćĢā
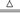 2Fe2O3+8SO2
2Fe2O3+8SO2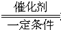 2SO3
2SO3 H2SO4
H2SO4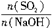 =x,ŹŌŠ“³öxŌŚ²»Ķ¬Č”Öµ·¶Ī§Ź±£¬n£ØNaHSO3£©µÄÖµ»ņn£ØNaHSO3£©Óėn£ØSO2£©”¢n£ØNaOH£©¼äµÄ¹ŲĻµŹ½”£
=x,ŹŌŠ“³öxŌŚ²»Ķ¬Č”Öµ·¶Ī§Ź±£¬n£ØNaHSO3£©µÄÖµ»ņn£ØNaHSO3£©Óėn£ØSO2£©”¢n£ØNaOH£©¼äµÄ¹ŲĻµŹ½”£| x=n£ØSO2£©/n£ØNaOH£© | n£ØNaHSO3£© |
| | |
| | |
| | |
 Na2SO3+H2O;NaOH+SO2
Na2SO3+H2O;NaOH+SO2  aHSO3”£øł¾ŻĢāøųĢõ¼ž£¬¶ŌÉĻŹö·“Ó¦ŌĖÓĆ¼«Öµ¼ŁÉč·Ø½ųŠŠ·ÖĪöĢÖĀŪ”£µŚ£Ø3£©²½æ¼²é¼ĘĖćĢāÖŠ·¶Ī§ĢÖĀŪµÄ»ł“”ÖŖŹ¶£¬ŅŌ¼°¹żĮæĪŹĢāŗĶĘ½ŠŠ·“Ó¦µÄ¼ĘĖć”£
aHSO3”£øł¾ŻĢāøųĢõ¼ž£¬¶ŌÉĻŹö·“Ó¦ŌĖÓĆ¼«Öµ¼ŁÉč·Ø½ųŠŠ·ÖĪöĢÖĀŪ”£µŚ£Ø3£©²½æ¼²é¼ĘĖćĢāÖŠ·¶Ī§ĢÖĀŪµÄ»ł“”ÖŖŹ¶£¬ŅŌ¼°¹żĮæĪŹĢāŗĶĘ½ŠŠ·“Ó¦µÄ¼ĘĖć”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®AgNO3ČÜŅŗ | B£®CuSO4ČÜŅŗ? |
| C£®Ļ”H2SO4 | D£®BaCl2ČÜŅŗ? |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ņņ·¢Éś”°¶Ū»Æ”±¶ų²»·“Ó¦ | B£®²śÉśµÄSO2ĪŖ0.100 mol |
| C£®²śÉśµÄSO2ÉŁÓŚ0.100 mol | D£®³żSO2Ķā»¹»įÓŠH2²śÉś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®SO2 | B£®H2S | C£®Cl2 | D£®CO |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com