
����Ŀ��ij�о���ѧϰС����̽������ɫ����������ˮ��Ӧ�Ƿų�����������������ʱ�������ͼ��ʾ��ʵ��װ�á�

��С�Թ������1g����ɫ�������ƣ���С�Թ����ڴ�֧�ܵ��Թ��ڡ���U�ι��ڼ���������īˮ����T�ι������У�ʹU�ι������ߵ�Һ�洦��ͬһˮƽ�档�ټн������У���ˮ����С�Թ��ڣ��ɹ۲쵽U�ι��Ҳ��Һ�������½�������Һ��������
��1���������Ƶĵ���ʽ__��
��2��д��������Ӧ�Ļ�ѧ����ʽ__��
��3�����и�ͼ�У���ʾ����������ˮ��Ӧ��ͼ����_______��
A.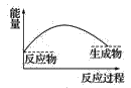 B.
B.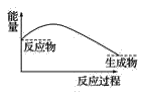
C.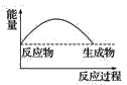 D.
D.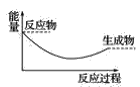
���𰸡�![]() 2Na2O2��2H2O=4NaOH��O2�� B
2Na2O2��2H2O=4NaOH��O2�� B
��������
�������������ӻ����������������������ԭ���γ�һ�Թ��õ��Ӷԣ�����������ˮ�ķ�Ӧ�Ƿ��ȷ�Ӧ����Ӧ����е��������������������������
��1���������������ӻ����������������������ԭ���γ�һ�Թ��õ��Ӷԣ��������Ƶĵ���ʽ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��2���������ƺ�ˮ��Ӧ�����������ƺ���������Ӧ�Ļ�ѧ����ʽ2Na2O2��2H2O=4NaOH��O2�����ʴ�Ϊ��2Na2O2��2H2O=4NaOH��O2����
��3������������ˮ�ķ�Ӧ�Ƿ��ȷ�Ӧ����Ӧ����е����������������������������ѡB���ʴ�Ϊ��B��


 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л�������9,10-�����ƵĽṹ��ͼ��ʾ�����й��ڸ����ʵ�˵����ȷ����

A. �����ʷ���ʽΪC16H12
B. ��������ױ���Ϊͬϵ��
C. ������������ˮ����ȡ����Ӧ�ͼӳɷ�Ӧ
D. �����ʱ��������ȴ����ͬ���칹����4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z��M��E��Q��Ϊϡ��������Ķ�����Ԫ�أ�����ԭ��������������X��������������W��4����Z��E��������ϼ���ͬ��X��M�����ڱ���λ����ͼ��
X | ||
M | E |
��1��Y�����ڱ��е�λ��Ϊ________��Q��Ԫ������Ϊ_______��
��2��X�����������ĵ���ʽΪ____________________��Y��W�γɵ�������ӵĵ���ʽΪ_________________��
��3������Ԫ��ԭ�Ӱ뾶�����ǣ�дԪ�ط��ţ�________��
��4��X��E������������ˮ���ﷴӦ�Ļ�ѧ��ӦʽΪ___________________________��
��5��������ʵ��˵��ZԪ�صķǽ����Ա�EԪ�صķǽ�����ǿ����________
��Z������E�ļ��⻯�����Һ��Ӧ����Һ�����
����������ԭ��Ӧ�У�1mol Z���ʱ�1mol E���ʵõ��Ӷ�
��Z��E��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�߷ֽ��¶ȸ�
��6��M��Q��Ԫ�صĵ�������1mol M����ۻ�����ָ������£�����687kJ����֪�û�������ܷе�ֱ�Ϊ��69����58����д���÷�Ӧ���Ȼ�ѧ����ʽ��_________
��7��ͭ��һ��Ũ�ȵ����������Ļ��ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���ɵ���������������Ԫ���е�����Ԫ����ɡ��������Է���������С��50��Ϊ��ֹ��Ⱦ����������������ȫת��Ϊ��ۺ����ᣬ����1L 2.2mol/L NaOH��Һ��1mol O2������������ķ���ʽ�Լ����ʵ����ֱ�Ϊ____________________�����ɵ�����ͭ�����ʵ���Ϊ____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
��1����25�桢101kPa�£�1g�״���CH3OH��ȼ������CO2��Һ̬ˮʱ����22.68kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ___��
��2��25�桢101kPa��������N2��O2��ȫ��Ӧ��ÿ����23gNO2��Ҫ����16.95kJ����___��
��3��25�桢101kPa��֪��1mol H��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ___��
��4���״�������Ҫ�Ļ���ԭ�ϣ��ֿ���Ϊȼ�ϡ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ��������ºϳɼ״�����������Ҫ��Ӧ���£�
��CO(g)+2H2(g)![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��CO2(g)+3H2(g)![]() CH3OH��g��+H2O(g) ��H2
CH3OH��g��+H2O(g) ��H2
��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H3
CO(g)+H2O(g) ��H3
�ش��������⣺
��֪��Ӧ������صĻ�ѧ�������������£�
��ѧ�� | H��H | C��O | C | H��O | C��H |
E/��kJ��mol-1�� | 436 | 343 | 1076 | 465 | 413 |
�ɴ˼�����H1=___kJ��mol-1����֪��H2=-58kJ��mol-1������H3=___kJ��mol-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������������ҪӰ�졣
(1)�����Ʊ������á�
�� ��ҵ�ϳɰ��Ļ�ѧ����ʽ��________��
�� ������������һ��������Ӧ�Ļ�ѧ����ʽ��________��
(1)���Ķ�����⡣
ˮ���а�����笠�����(ͳ�ư���)�����ļ�ⱸ�ܹ�ע�����ð������������ˮ���а���������ʾ��ͼ��

�� ����ƽ��ԭ������������ˮ���м���NaOH��Һ�����ã�________��
�� �����ð�����������1 Lˮ���еİ�����ȫת��ΪN2ʱ��ת�Ƶ��ӵ����ʵ���Ϊ6��10-4 mol��L-1����ˮ���а���(������)����Ϊ________mg��L-1��
(3)����ת����ȥ����
����ȼ�ϵ��(MFC)��һ���ִ�������ȥ����������ͼΪMFC̼������ͬʱȥ���ĵ�ת��ϵͳԭ��ʾ��ͼ��
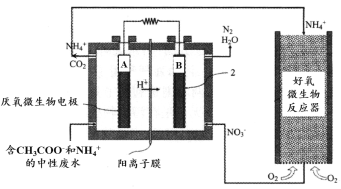
�� ��֪A��B��������CO2��N2�����ʵ���֮��Ϊ5 : 2��д��A���ĵ缫��Ӧʽ��________��
�� �û�ѧ�������NH4+ȥ����ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Fe3O4�ڴ����塢������ҽѧ��������й�����Ӧ��ǰ���������������Ʊ�����Fe3O4�ķ������£�
I��Fe2+����������FeSO4��Һ��NaOH��Һ����pH��a���ټ���H2O2��Һ�������õ� FeO( OH)����ɫ����Һ��
��1��������NaOH��Һ����pH��������Ұ�ɫ�������÷�Ӧ�����ӷ���ʽ�� _____________��
��������Ӧ��ɺ��aֵ��FeO(OH)���ʼ������ɺ���ҺpH�Ĺ�ϵ��������£�
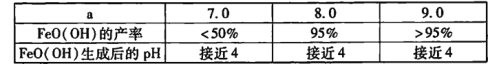
�����ӷ���ʽ����FeO( OH)���ɺ���ҺpH�½���ԭ��____��
��2�������飺��a=7ʱ�������д��ڴ���Fe2O3����Fe2 O3�IJ���������ּ��裺
i����Ӧ��������Һ������ǿ������FeO( OH)��Fe2 O3��ת����
ii����Һ�д�������Fe2+������FeO( OH)��Fe2O3��ת����
��������������i��������ʵ��������____��
������������ͬʱ����FeO( OH)��Һ�м��벻ͬŨ��Fe2+��30 min��ⶨ���ʵ���ɣ�������£�
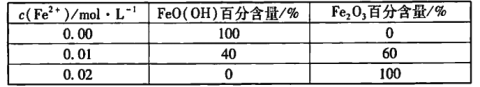
���Ͻ��������____��
�� a=7��a =9ʱ��FeO( OH)���ʲ���ܴ��ԭ����____��
����Fe2+��Fe3+����������FeO( OH)����ɫ����Һ��ͬʱ����FeSO4��Һ��NaOHŨ��Һ���й��������ٽ��˻��Һ���Ȼ�������ȴ�����ˡ�ϴ�ӡ�����õ�����Fe3O4��
��3��������ʱ�ķ�Ӧ�����Բ��﴿�ȺͲ��ʵ�Ӱ�켫��
��������pH����ʱ���ᵼ��FeSO4��Һ������������������pH����ʱ���õ�������Fe3O4�л���е�������____��
����֪N=n[FeO(OH)]/n(Fe2+)����������һ��ʱ���������Fe3O4�IJ�����N�ı仯��������ͼ��ʾ��

�����۷�����N=2������ʱ����Fe3O4����Ӧ��ߣ���ʵ������˵Ŀ���ԭ����_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��ʵ�����н�������ʵ�飺
��� | �� | �� | �� |
ʵ�� |
|
|
|
���� | û�����Ա仯����Һ��Ϊ��ɫ | �г������ɣ���ҺΪ����ɫ | ����ɫ���ݲ��� |
���½��۲���ȷ���ǣ� ��
A.���������Ա仯��˵������Һ����Ӧ
B.���еİ�ɫ����ΪBaSO4
C.���з����ķ�Ӧ�����ӷ�Ӧ
D.���з�����Ӧ�����ӷ���ʽΪ2H����Zn��Zn2����H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ�������������



�� �� ��
A. ͼ���д�ˮ�������¶ȣ��Ϳ��Դ�a��䵽c��
B. ͼ������b���Ӧ�¶��£���pH=2��H2SO4��Һ��pH=10��NaOH��Һ�������Ϻ���Һ������
C. ͼ�ұ���ͬ�¶���pH=1������ʹ�����Һ�ֱ��ˮϡ��ʱpH�ı仯���ߣ��������ߢ�Ϊ���ᣬ��b����Һ�ĵ����Ա�a��ǿ
D. ��0.0100mol/L����������Һ,�ζ�Ũ�Ⱦ�Ϊ0.1000mol/L��C1-��Br-��I-�Ļ����Һ����ͼ�����ߣ���ȷ�����ȳ�������Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ϊ����ͭ��֮�����������˴��۶���ë������ɢ���̵����������ͭ�����о���ͭ������Cu��Sn�ȣ��ڳ�ʪ�����з����ĸ�ʴ�������ﱣ����������Ҫ���塣��ͼΪ��ͭ���ڳ�ʪ�����з����绯ѧ��ʴ��ԭ��ʾ��ͼ������˵������ȷ����
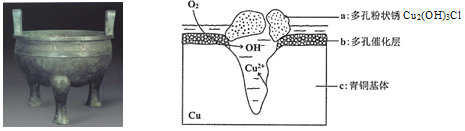
A. ��ͭ�������绯ѧ��ʴ��ͼ��c��������������
B. ���������ĵ缫��ӦΪO2+ 4e��+2H2O=4OH��
C. �����е�Cl�� ��������������Ӧ�IJ�����������a�����ӷ���ʽΪ2Cu2��+3OH��+Cl��=Cu2 (OH)3Cl��
D. ������0.2 mol Cu2(OH)3Cl�������������ĵ�O2���Ϊ4.48L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com