
在2 L密闭容器内,800℃时反应:2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800℃,反应达到平衡时,NO的物质的量浓度是__________;升高温度,NO的浓度增大,则该反应是________(填“放热”或“吸热”)反应。
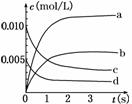
(2)如图中表示NO2变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________。
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
解析:(1)平衡时,n(NO)=0.007 mol,c(NO)= =0.003 5 mol/L。升高温度,c(NO)增大,则平衡左移,正反应是放热反应。
=0.003 5 mol/L。升高温度,c(NO)增大,则平衡左移,正反应是放热反应。
(2)从n(NO)随时间变化表可得出,NO的物质的量随时间的推移而减小,NO与O2是反应物,NO2是生成物,NO2的变化曲线只能是a、b中的某一条。反应在3 s之后,NO的物质的量不再发生变化,反应过程中NO减小0.013 mol,根据方程式可知NO2增加0.013 mol,而容器体积2 L,所以达到平衡时,NO2的浓度0.006 5 mol/L,曲线b符合。0~2 s内,NO减少0.012 mol,据反应方程式,O2同时减少0.006 mol,以O2来表示这段时间的平均速率=0.006 mol÷2 L÷2 s=0.001 5 mol/(L·s)。
(3)a项在达没达到平衡都成立,因为反应速率之比等于化学计量数之比。反应2NO(g)+O2(g)  2NO2(g)的反应前后气体分子数目不相等,平衡受压强的影响,压强改变,平衡要移动,b项中压强已保持不变,所以b项已达平衡状态。根据平衡状态的定义,正逆反应速率相等可得c项也达平衡状态。密度等于质量除以体积,该反应的反应物和生成物均为气体,质量不变,而容器的体积2 L,也不发生变化,所以任何条件下密度都不发生改变,d项不能说明反应是否达到平衡状态。
2NO2(g)的反应前后气体分子数目不相等,平衡受压强的影响,压强改变,平衡要移动,b项中压强已保持不变,所以b项已达平衡状态。根据平衡状态的定义,正逆反应速率相等可得c项也达平衡状态。密度等于质量除以体积,该反应的反应物和生成物均为气体,质量不变,而容器的体积2 L,也不发生变化,所以任何条件下密度都不发生改变,d项不能说明反应是否达到平衡状态。
(4)分离出NO2气体,反应速率减慢,加入催化剂,平衡不移动,升高温度该反应向逆反应方向移动,所以a、b、d均错误。增大反应物O2的浓度,反应速率增大,平衡向正反应方向移动,c正确。
答案:(1)0.003 5 mol/L 放热
(2)b 1.5×10-3 mol/(L·s)
(3)b、c
(4)c


科目:高中化学 来源: 题型:
某同学用Na2CO3配制0.10 mol·L-1Na2CO3(aq),其称量操作如下图所示,最终配制溶液的浓度

A.偏高 B.偏低
C.可能偏高也可能偏低 D.准确
查看答案和解析>>
科目:高中化学 来源: 题型:
分类法在化学的发展中起到非常重要的作用,下列分类标准合理的是
①根据氧化物的组成元素将氧化物分成酸性氧化物、碱性氧化物和两性氧化物
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否有丁达尔效应将分散系分为溶液、胶体和浊液
④根据反应中的热效应将化学反应分为放热和吸热反应
⑤根据水溶液能否导电将化合物分为电解质和非电解质
A.②④ B. ②③④ C. ①③⑤ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
NaCl是一种化工原料,可以制备一系列物质(如图所示)。
下列说法正确的是
A.常温下干燥Cl2能用钢瓶贮运,所以Cl2与铁不反应
B.25℃,NaHCO3在水中的溶解度比Na2CO3的大
C.源石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂
D.图中所示转化反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应限度的说法中正确的是( )
A.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度
B.当一个可逆反应达到平衡状态时,正反应速率和逆反应速率相等但不等于0
C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变
D.化学反应的限度不可以通过改变条件而改变
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(g)+bB(g)  cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )
cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )

A.a+b>c+d T1>T2 ΔH>0
B.a+b>c+d T1<T2 ΔH<0
C.a+b<c+d T1>T2 ΔH>0
D.a+b<c+d T1<T2 ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g)
该温度下,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,则10 min内CO2的平均反应速率为0.015 mol/(L·min),10 min后生成了单质铁________g。
(2)可用上述反应中某种物理量来说明该反应已达到平衡状态的是______________。
A.CO的生成速率与CO2的生成速率相等
B.CO生成速率与CO2消耗速率相等
C.CO的质量不变
D.体系的压强不再发生变化
E.气体密度不再变化
(3)写出氢氧化铝在水中发生酸式电离的电离方程式;
________________________________________________________________________。
欲使上述体系中H+浓度增大,可加入的物质是________。
A.NaOH B.HCl
C.NH3 D.NaHSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释实验事实的离子方程式正确的是
A.将Na2O2固体投入H O中:
O中:
2Na2O2+2H O===4Na++4OH-+18O2↑
O===4Na++4OH-+18O2↑
B.明矾溶液中加入Ba(OH)2溶液至生成的沉淀物质的量最多:
Al3++2SO +2Ba2++3OH-===Al(OH)3↓+2BaSO4↓
+2Ba2++3OH-===Al(OH)3↓+2BaSO4↓
C.误将洁厕灵与消毒液混合:
2H++Cl-+ClO-===Cl2↑+H2O
D.用惰性电极电解CuCl2溶液:
2Cl-+2H2O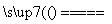 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下的2 L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示。下列说法正确的是( )
| X | Y | W | |
| n(起始状态)/mol | 2 | 1 | 0 |
| n(平衡状态)/mol | 1 | 0.5 | 1.5 |
A.该温度下,此反应的平衡常数表达式是K=
B.升高温度,若W的体积分数减小,则此反应ΔH>0
C.增大压强,正、逆反应速率均增大,平衡向正反应方向移动
D.该温度下,再向容器中通入3 mol W,达到平衡时,n(X)=2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com