
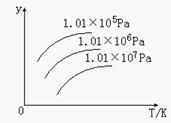
右图表示温度、压强对下列平衡的影响:N2 (g)+3H2(g)  2NH3(g) △H<0
2NH3(g) △H<0
图中y轴表示的意义是( )
A. 正反应速率
B. 平衡混合气体中NH3的含量
C. 平衡混合气体中N2的物质的量
D. H2的转化率
科目:高中化学 来源: 题型:
性质决定用途,化学知识运用得当可以使人类的生活更美好。下列物质性质与应
用的对应关系正确的是
A.氢氧化铝具有弱碱性,可用于制胃酸中和剂
B.浓硫酸具有酸性,可用于刻蚀玻璃制品
C.漂白粉在空气中不稳定,可用于漂白纸张
D.晶体硅熔点高硬度大,可用于制作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
将溶质的质量分数为14%的KOH溶液加热蒸发掉100 g水后,得到溶质的质量分数为28%的溶液80 mL,此时溶液的物质的量浓度为( )
A.5 mol·L-1 B.6.25 mol·L-1
C.7 mol·L-1 D.6.75 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
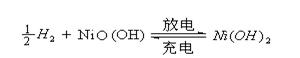 氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。氢镍电池的总反应式是
氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。氢镍电池的总反应式是
根据此反应式判断,下列叙述中正确的是 ( )
A.电池放电时,电池负极周围溶液的PH不断增大
B.电池放电时,镍元素被氧化
C.电池充电时,氢元素被还原 D.电池放电时,氢气是正极
查看答案和解析>>
科目:高中化学 来源: 题型:
一真空定容的密闭容器中盛有1mol PCl5,发生反应PCl5(g) 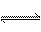 PCl3(g)+Cl2(g),一定条件下平衡时PCl5所占的体积百分数为M,若相同条件相同容器中,最初放入2 mol PCl5,则平衡时,PCl5的体积百分数为N,下列结论正确的是( )
PCl3(g)+Cl2(g),一定条件下平衡时PCl5所占的体积百分数为M,若相同条件相同容器中,最初放入2 mol PCl5,则平衡时,PCl5的体积百分数为N,下列结论正确的是( )
A.M>N B.M=N C.M<N D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
800℃时,在2L密闭容器中发生2NO(g)+O2(g)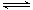 2NO2(g),测得n(NO)随时间的变化如下表:
2NO2(g),测得n(NO)随时间的变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)用O2表示2s时该反应的平均速率v =__________________。
(2)写出该反应的平衡常数表达式:K=__________________________ ___ 。已知:K(800℃)>K(850℃),该反应是__________(填“吸热”或“放热”)反应。
(3)能说明该反应已经达到平衡状态的是___________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内气体的密度保持不变
(4)下列操作中,能使该反应的反应速率增大,且平衡向正反应方向移动的是_______。
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效的催化剂
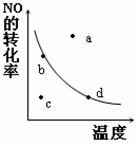
(5)下图中的曲线表示的是其他条件一定时,反应:2NO (g)+O2(g) 2NO2(g)中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 。
2NO2(g)中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 。
A.a点 B.b点
C.c点 D.d点
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除去杂质的方法正确的是( )
A.除去N2中的少量O2:通过灼热的CuO粉,收集气体
B.除去CO2中的少量水蒸气:通入装有碱石灰的干燥管,收集气体
C.除去FeCl2溶液中的少量CuCl2:加入过量铁屑,充分反应后,过滤
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
欲测定某生铁(主要成分是铁,还含有少量的碳)的组成,进行了如下实验:
称取粉末状样品8.5克,加入某浓度的盐酸100 mL ,充分反应后,收集到标准状况下气
体2.24 L ;然后,继续往样品中加入同浓度的盐酸100mL ,充分反应后又收集到标准
状况下气体1.12 L 。
试求:(写出具体计算过程)
(1)所取盐酸的物质的量浓度。
(2)该生铁样品中碳的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.用惰性电极电解饱和氯化钠溶液:2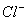 + 2H+
+ 2H+  H2↑+ Cl2↑
H2↑+ Cl2↑
B.用银氨溶液检验乙醛中的醛基:
CH3CHO +2Ag(NH3)2+ + 2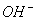

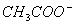 +
+ 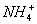 +3NH3 + 3Ag↓+ H2O
+3NH3 + 3Ag↓+ H2O
C.苯酚钠溶液中通入少量CO2:CO2 + H2O + 2C6H5O- 2C6H5OH + 2
2C6H5OH + 2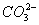
D.Na2SO3溶液使酸性KMnO4溶液褪色:5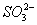 + 6H+ + 2MnO4- == 5
+ 6H+ + 2MnO4- == 5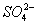 + 2Mn2+ 3H2O
+ 2Mn2+ 3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com