
【题目】如图装置,电流计指针会偏转,正极变粗,负极变细,符合这种情况的是

A. 正极:Cu 负极:Zn S:稀H2SO4
B. 正极:Zn 负极:Cu S:CuSO4溶液
C. 正极:Ag 负极:Zn S:AgNO3溶液
D. 正极:Fe 负极:Cu S:AgNO3溶液
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
I. 利用反应:6NO2 + 8NH3![]() 7N2 + 12 H2O处理NO2。
7N2 + 12 H2O处理NO2。
II. 一定条件下NO2与SO2可发生反应:NO2(g)+SO2(g)![]() SO3(g)+NO(g) Q (Q>0) 。
SO3(g)+NO(g) Q (Q>0) 。
III. CO可用于合成甲醇,反应方程式为:CO(g) + 2H2(g)![]() CH3OH(g) 。
CH3OH(g) 。
(1)硫离子最外层电子的电子排布式为__________________,氨气分子的电子式为___________,氨气分子属于___________分子(填“极性”或者“非极性”)。
(2)C、O、S、N这四种元素中属于同周期元素的非金属性由强到弱的顺序为_______________,能证明其递变规律的事实是(________)
a、最高价氧化物对应水化物的酸性 b、气态氢化物的沸点
c、单质与氢气反应的难易程度 d、其两两组合形成的化合物中元素的化合价
(3)对于I中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均反应速率υ(NO2) =_______________。
(4)对于II中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是_____________
a. 体系压强保持不变 b. NO2浓度保持不变
c. NO2和SO3的体积比保持不变 d. 混合气体的平均相对分子质量保持不变
(5)请写出II中反应的平衡常数表达式K=_____________________________________。如果II中反应的平衡常数K值变大,该反应___________
a.一定向正反应方向移动 b. 平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d. 平衡移动时,逆反应速率先增大后减小
(6)对于III中的反应,CO在不同温度下的平衡转化率与压强的关系如图示。实际生产条件控制在250℃、1.3×104 kPa左右,简述选择此压强的理由:____________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研机构以纳米Fe2O3作为电极材料制备锂离子电池另一极为金属锂和石墨的复合材料,电解质只传导锂离子,通过在宝温条件下对锂离于电池进行循环充放电,成功实现了对磁性的可逆调控(见图)。下列说法正确的是

A. 电解质可以用Li2SO4溶液
B. 充电时,Fe作为阴极,电池不被磁铁吸引
C. 放电时,正极反应为Fe2O3+6Li++6e-==2Fe+3Li2O
D. 充电时,阴极反应为:Li2O +2e-==2Li+O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在水中大量共存的一组离子是
A.NH4+、Na+、Cl-、SO42-B.H+、Na+、NO3-、CO32-
C.K+、Ba2+、OH-、SO42-D.K+、Ag+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常检测SO2含量是否达到排放标准的反应原理是SO2 +H2O2 + BaCl2 ===BaSO4↓+ 2HCl。NA表示阿伏伽德罗常数,下列说法正确的是( )
A. 0.1 mol BaCl2晶体中所含微粒总数为0.1NA
B. 25 ℃时,pH =1的HCl溶液中含有H+的数目为0.1NA
C. 17 g H2O2中含有非极性键数目为0.5NA
D. 生成2.33 g BaSO4沉淀时,转移电子数目为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. CH2Cl2有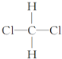 和
和 两种结构
两种结构
B. 分子式为C3H6和C5H10的物质一定互为同系物
C.  的一氯代物有5种
的一氯代物有5种
D. 1mol某烷烃完全燃绕消耗11molO2,则其主链上含有5个碳原子的同分异构体(不考虑空间异构)有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬铁矿的成分主要为FeCr2O4,另含有少量Al2O3和SiO2。从铬铁矿中提取铁、铬的化合物,并获得副产物的工艺流程如下:
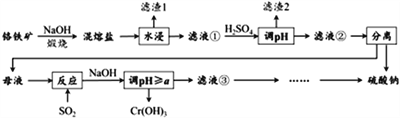
已知“混熔盐”中含有Na2CrO4和NaFeO2等成分,其中NaFeO2极易水解。试回答下列问题:
(1)“滤渣1”为红褐色沉淀,其化学式为_________________;通过水浸生成红褐色沉淀的化学方程式为_________________________________。
(2)向滤液①中加H2SO4“调“pH”的目的:一是使CrO42-转化为Cr2O72-,离子方程式为___________________________________;二是____________________________。
(3)“煅烧”铬铁矿时,主要成分反应的化学方程式为____________________________。
(4)根据下图溶解度(S)~温度(T)曲线判断,对滤液②进行的最佳“分离”方法为_____________(填序号)。
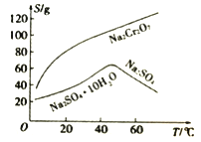
A.蒸发结晶 B.蒸发浓缩,趁热过滤 C.蒸发浓缩,冷却结晶,过滤
(5)“反应”的离子方程式为____________________________。
(6)Cr(OH)3溶于盐酸生成配离子[CrCln(H2O)6-n]x+。0.0015mol[CrCln(H2O)6-n]x+与氢离子交换树脂(HR)完全发生离子交换:[CrCln(H2O)6-n]x++xHR→Rx[CrCln(H2O)6-n] +xH+,生成的H+可与25.00mL 0.1200mol/L NaOH溶液恰好中和。则该配离子的化学式为__________________。
(7)已知25℃时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=1.0×10-32。则使Cr3+恰好完全沉淀,即溶液中c(Cr3+)=1.0×10-5mol/L时,应调节pH的最小值a为多少___________?(列式计算)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时N电极的质量减少,请回答下列问题: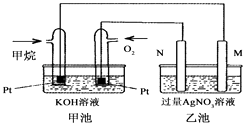
(1)M电极的材料是 , 其电极反应式为:N的电极名称是 , 电极反应式为:
(2)通入甲烷的铂电极的电极反应式为 .
(3)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为 L(标准状况下).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com