
【题目】Na3OCl是一种良好的离子导体,具有反钙钛矿晶体结构。回答下列问题:
(1)Ca小于Ti的是_______(填标号)。
A.最外层电子数 B.未成对电子数 C.原子半径 D.第三电离能
(2)由O、Cl元素可组成不同的单质和化合物,其中Cl2O2能破坏臭氧层。
① Cl2O2的沸点比H2O2低,原因是___________________________________。
② O3分子中心原子杂化类型为_______;O3是极性分子,理由是___________________。
(3)Na3OCl可由以下两种方法制得:
方法Ⅰ Na2O + NaCl![]() Na3OCl
Na3OCl
方法II 2Na + 2NaOH + 2NaCl![]() 2Na3OCl + H2↑
2Na3OCl + H2↑
① Na2O的电子式为____________。
② 在方法Ⅱ的反应中,形成的化学键有_______(填标号)。
A.金属键 B.离子键 C.配位键 D.极性键 E.非极性键
(4)Na3OCl晶体属于立方晶系,其晶胞结构如右所示。已知:晶胞参数为a nm,密度为d g·cm-3。
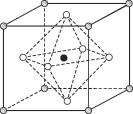
①Na3OCl晶胞中,Cl位于各顶点位置,Na位于_________位置,两个Na之间的最短距离为________nm。
②用a、d表示阿伏加德罗常数的值NA=__________________(列计算式)。
【答案】B H2O2分子间存在氢键 sp2 O3分子为V形结构(或“O3分子中正负电荷重心不重合”等其他合理答案) ![]() BE 面心
BE 面心 ![]()
![]()
【解析】
(1)基态Ca原子核外电子排布为1s22s22p63s23p64s2,基态Ti原子核外电子排布为1s22s22p63s23p63d24s2,结合元素周期律分析判断;
(2)①同种类型晶体的熔沸点高低取决于微粒间作用力的大小,分子间存在氢键的熔沸点高;②根据价层电子对互斥理论和杂化轨道理论分析解答;
(3)Na2O为离子化合物,据此书写其电子式;根据Na3OCl和H2存在的化学键类型判断;
(4)①根据均摊法分析判断Na3OCl晶体结构中空心白球、顶点阴影球、实心黑球的数目再结合Na3OCl化学式分析判断;②由密度公式ρ=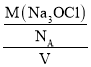 计算解答。
计算解答。
(1)基态Ca原子核外电子排布为1s22s22p63s23p64s2,未成对电子数为0,基态Ti原子核外电子排布为1s22s22p63s23p63d24s2,未成对电子数为2。A.最外层电子数相等,错误;B.Ca的未成对电子数小于Ti,正确;C.同一周期元素,原子序数小的原子半径大,原子半径Ca原子略大,错误;D.Ca原子失去两个电子后恰好达到全满结构,很难失去第三个电子,第三电离能Ca较大,错误,故答案为:B;
(2)①同种类型晶体的熔沸点高低取决于微粒间作用力的大小,H2O2分子间存在氢键,熔沸点高,故答案为:H2O2分子间存在氢键;
②根据价层电子对互斥理论,O3分子的中心O原子的价层电子对为2+![]() (6-2×2)=3,杂化形式为sp2,O3分子为V形结构,分子中正负电荷重心不重合,为极性分子,故答案为:sp2;O3分子为V形结构(或O3分子中正负电荷重心不重合);
(6-2×2)=3,杂化形式为sp2,O3分子为V形结构,分子中正负电荷重心不重合,为极性分子,故答案为:sp2;O3分子为V形结构(或O3分子中正负电荷重心不重合);
(3)①Na2O属于离子化合物,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
②在方法Ⅱ的反应中,形成的化学键有Na3OCl中Na与O、Na与Cl间的离子键,H2分子内有H与H间的非极性键,故答案为:BE;
(4)①Na3OCl晶体结构中空心白球类原子6×![]() =3、顶点阴影球类原子8×
=3、顶点阴影球类原子8×![]() =1、实心黑球类原子1×1=1,根据Na3OCl化学式,可判断钠原子应为空心白球,处在晶体结构的面心,两个钠原子之间的最短距离为晶体结构中两个面心的距离,即为一半边长的
=1、实心黑球类原子1×1=1,根据Na3OCl化学式,可判断钠原子应为空心白球,处在晶体结构的面心,两个钠原子之间的最短距离为晶体结构中两个面心的距离,即为一半边长的![]() 倍,即
倍,即![]() a nm,故答案为:面心;
a nm,故答案为:面心;![]() a;
a;
②已知:晶胞参数为anm,密度为dgcm-3,则dgcm-3=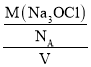 =
=![]() ,解得:NA=
,解得:NA=![]() ,故答案为:
,故答案为:![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不合理的是( )

A. 用a趁热过滤提纯苯甲酸B. 用b制备并检验乙烯
C. 用c除去溴苯中的苯D. 用d分离硝基苯与水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核电站遭破坏,会造成放射性物质![]() I和
I和![]() Cs向外界泄漏。下列有关说法错误的是( )
Cs向外界泄漏。下列有关说法错误的是( )
A.每个![]() Cs含有78个中子
Cs含有78个中子
B.CsOH的碱性比KOH的强
C.HI的还原性比HF的强
D.KIO3是碘的最高价含氧酸的盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,其中NH3被氧化为常见的无毒物质。下列说法错误的是( )

A. 溶液中OH-向电极a移动
B. 电极b上发生还原反应
C. 负极的电极反应为2NH3-6e-+6OH-![]() N2+6H2O
N2+6H2O
D. 理论反应消耗的NH3与O2的物质的量之比为3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019 年诺贝尔化学奖授予三位开发锂离子电池的科学家。TiS2、LiCoO2 和 LiMnO2 等都是他们研究锂离子电池的载体。回答下列问题:
(1)基态 Ti 原子的价层电子排布图为____。
(2)在第四周期 d 区元素中,与 Ti 原子未成对电子数相同的元素名称________。
(3)金属钛的原子堆积方式如图所示,则金属钛晶胞俯视图为______。
![]()
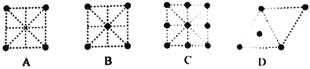
(4)已知第三电离能数据:I3(Mn)=3246 kJ·mol-1,I3(Fe)=2957 kJ·mol-1。锰的第三电离能大于铁的第三电离能,其主要原因是______。
(5)据报道,在 MnO2 的催化下,甲醛可被氧化成 CO2,在处理含 HCHO 的废水或空气方面有广泛应用。HCHO中键角________CO2 中键角(填“大于”“小于”或“等于”)。
(6)Co3+、Co2+能与 NH3、H2O、SCN-等配体组成配合物。
①1 mol[ Co(NH3)6]3+含______mol σ键。
②配位原子提供孤电子对与电负性有关,电负性越大,对孤电子对吸引力越大。SCN-的结构式为[S=C=N] -,SCN-与金属离子形成的配离子中配位原子是_______(填元素符号)。
(7)工业上,采用电解熔融氯化锂制备锂,钠还原 TiCl4(g)制备钛。已知:LiCl、TiCl4的熔点分别为 605℃、-24℃,它们的熔点相差很大,其主要原因是________。
(8)钛的化合物晶胞如图所示。
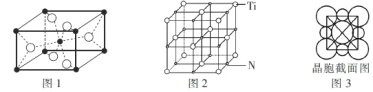
二氧化钛晶胞如图 1 所示,钛原子配位数为______。氮化钛的晶胞如图 2 所示, 图 3 是氮化钛的晶胞截面图(相邻原子两两相切)。已知:NA 是阿伏加德罗常数的值,氮化钛晶体密度为 d g·cm-3。氮化钛晶胞中 N 原子半径为________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示。
元素 | 原子结构或性质 |
A | 原子最外层电子数是内层电子总数的1/5 |
B | 形成化合物种类最多的元素,其单质为固体 |
C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
D | 地壳中含量最多的元素 |
E | 与D同主族 |
F | 与E同周期,且最外层电子数等于电子层数 |
请回答下列问题:(用对应的化学用语回答)
(1)B在元素周期表中的位置是__________;用电子式表示A和E形成的化合物的形成过程 。
(2)A、 D 、E、 F离子半径由大到小的顺序为________________________________。
(3)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是__________________;
(4)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是____________________。该反应为 反应。(填“吸热”或“放热”)
(5)F的最高价氧化物与E的最高价氧化物的水化物反应的离子方程式为 。
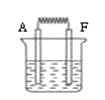
(6)如图:将A和F的单质与烧碱液构成原电池,负极的电极反应式为 ;外电路中电子从 电极流向 电极 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是_____。非金属性最强的元素的原子结构示意图为______。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是___________。
(3)②③④的原子半径由大到小的顺序是_________。
(4)元素⑦的氢化物常温下和元素②的单质反应的子方程式是________。
(5)⑧的最高价氧化物对应的水化物化学式为__________。
(6)①、⑥和⑦形成的化合物的化学式为______。该化合物的化学键类型为_________。
(7)⑧⑨三种元素形成的气态氢化物最稳定的是_______。
(8)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为________。
(9)下列可以判断①和⑤金属性强弱的是_______________。
a. ①单质的熔点比⑤单质低
b. ①质软,氧化物种类比⑤多
c. ①单质与水反应,⑤单质几乎不与水反应
d. ①最高价氧化物的水化物的碱性比⑤强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将所列仪器组装为一套实验室蒸馏石油的装置并进行蒸馏,可得到汽油和煤油。

(1)图中A、B、C三种仪器的名称分别是:A、______;B、______;C、______。
(2)将以上仪器按(一)→(六)顺序,用字母a,b,c…表示连接顺序:
e接____;h接____;k接l;b接____;____接____。
(3)A仪器中的c口用于______,d口用于______。
(4)蒸馏时,温度计水银球的位置应在________________。
(5)在B中注入原油后,加几片碎瓷片的目的是________________。
(6)给B加热,收集到沸点为60℃~150℃间的馏分是______,收集到150℃~300℃间的馏分是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料.它的发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:
SiO2![]() Si(粗)
Si(粗)![]() SiHCl3
SiHCl3![]() Si(纯)
Si(纯)
下列说法正确的是()
A.步骤①的化学方程式为:SiO2+C![]() Si+CO2↑
Si+CO2↑
B.SiO2既能与HF反应,又能与NaOH反应,所以SiO2属于两性氧化物
C.高纯硅是制造太阳能电池的常用材料,二氧化硅是制造光导纤维的基本原料
D.含硅化合物硅酸钠属于盐类,不属于碱,可以保存在磨口玻璃塞试剂瓶中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com