
| A. | ②④ | B. | ②③④ | C. | ②⑥ | D. | ③⑧ |
分析 可逆反应达到平衡状态时,同一物质的正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、百分含量以及由此引起的一系列物理量不变,据此分析解答.
解答 解:①C的生成速率与C的分解速率相等,说明C的正逆反应速率相等,该反应达到平衡状态,故正确;
②无论是否达到平衡,总存在单位时间内生成a molA、同时生成3a molB,所以不能据此判断平衡状态,故错误;
③A、B、C的分子数之比为1:3:2时,该反应不一定达到平衡状态,与反应初始浓度及转化率有关,所以不能据此判断平衡状态,故错误;
④任何化学反应中都存在质量守恒,所以无论反应是否达到平衡状态,A、B、C的总质量不变,所以不能据此判断平衡状态,故错误;
⑤反应前后气体的物质的量减少导致压强减小,当混合气体的总压强不再变化时,各物质的物质的量之和不变,该反应达到平衡状态,故正确;
⑥反应前后气体的物质的量减少,当混合气体的总物质的量不再变化时,该物质的物质的量不变,该反应达到平衡状态,故正确;
⑦单位时间内消耗a mol A,同时生成3a mol B,同时生成amolA,则A正逆反应速率相等,该反应达到平衡状态,故正确;
⑧A、B、C的浓度不再变化时,正逆反应速率相等,该反应达到平衡状态,故正确;
故选B.
点评 本题考查化学平衡状态的判断,为高频考点,侧重考查学生对化学平衡状态判断方法的理解、掌握和运用,只有反应前后改变的物理量才能作为化学平衡状态判断依据,题目难度不大.


 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:实验题
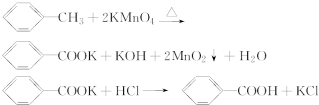
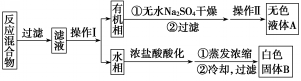
| 序号 | 实验方案 | 实验现象 | 结果 |
| ① | 将白色固体B加入水中,加热溶解,冷却结晶,过滤 | 得到白色晶体和无色滤液 | |
| ② | 取少量滤液于试管中,滴入适量的硝酸酸化的AgNO3溶液 | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体,取适量加热,测定熔点 | 白色晶体在122.4℃熔化为液体 | 白色晶体是苯甲酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2LCO和2LCO2 | B. | 9g H2O和标准状况下11.2LCO2 | ||
| C. | 标准状况下1molO2和22.4LH2O | D. | 0.2molH2和22.4LHCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
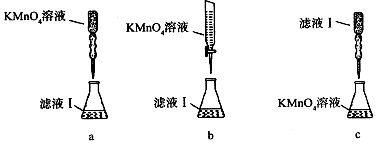
| A. | 用水洗涤2~3次后再使用 | |
| B. | 用滤纸擦干后才可使用 | |
| C. | 用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用 | |
| D. | 用盐酸洗涤后,经蒸馏水冲洗,方可使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯酸钾是还原剂 | |
| B. | KCl既是氧化产物,又是还原产物 | |
| C. | 反应中消耗3mol P时,转移电子的物质的量为15mol | |
| D. | 发令时产生的白烟只是KCl固体颗粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com