
向某盛有7.8gNa2O2的密闭容器中(无空气)通入4.48LNO2(标准状况),然后注入200mL水,充分反应后,容器中所含物质有()
A. NaNO2 NO H2O
B. NaNO3 NaOH O2 H2O
C. NaNO3 H2O
D. NaNO3 HNO3 O2 H2O
考点: 有关混合物反应的计算.
分析: n(Na2O2)= =0.1mol,n(NO2)=
=0.1mol,n(NO2)=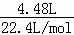 =0.2mol,二者发生氧化还原反应,反应方程式为Na2O2+2NO2=2NaNO3,根据方程式知,二者恰好反应,据此分析解答.
=0.2mol,二者发生氧化还原反应,反应方程式为Na2O2+2NO2=2NaNO3,根据方程式知,二者恰好反应,据此分析解答.
解答: 解:n(Na2O2)= =0.1mol,n(NO2)=
=0.1mol,n(NO2)=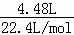 =0.2mol,n(Na2O2):n(NO2)=0.1mol:0.2mol=1:2,二者发生氧化还原反应,反应方程式为 Na2O2+2NO2=2NaNO3,根据方程式知,二者恰好反应生成NaNO3,所以充分反应后,容器中所含物质有NaNO3、H2O,
=0.2mol,n(Na2O2):n(NO2)=0.1mol:0.2mol=1:2,二者发生氧化还原反应,反应方程式为 Na2O2+2NO2=2NaNO3,根据方程式知,二者恰好反应生成NaNO3,所以充分反应后,容器中所含物质有NaNO3、H2O,
故选C.
点评: 本题考查混合物的计算,侧重考查分析计算能力,正确书写二者反应方程式是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:
与50mL 0.1mol﹣1 Na2CO3溶液中Na+的物质的量浓度相同的溶液是()
A. 50mL 0.2mol•L﹣1的NaCl溶液
B. 100mL 0.1mol•L﹣1的NaCl溶液
C. 25mL 0.2mol•L﹣1的Na2SO4溶液
D. 10mL 0.5mol•L﹣1的Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
有机化合物中当某一碳原子同时连在两个﹣OH是一种不稳定结构,会自动转化为稳定结构,例如: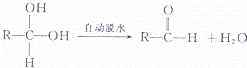
现有分子式为C9H8O2X2(X为一未知元素)的物质M,可在一定条件下发生下列反应:
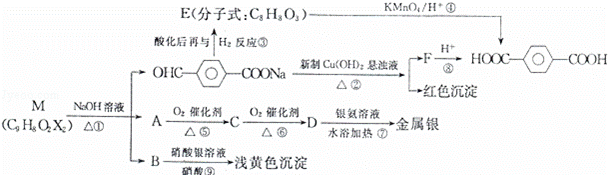
试回答下列问题:
(1)X为Br(填元素符号);反应①的反应类型是 .
(2)写出M的结构简式: .
(3)写出由A→C的化学反应方程式: .
(4)写出与E互为同分异构体,且同时符合下列四个条件的有机物的结构简式: 、 .
①含酯基;②含酚羟基;③不能发生银镜反应;④苯环上的一氯取代物只有2种.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是()
A. 硫酸铝溶液中加入过量氨水 Al3++3OH﹣═Al(OH)3↓
B. 电解饱和食盐水 2Cl﹣+2H2O  H2↑+C12↑+2OH﹣
H2↑+C12↑+2OH﹣
C. 碳酸钙与醋酸反应 CaCO3+2H+═Ca2++CO2↑+H2O
D. 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液 Fe2++2H++H2O2═Fe3++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液中存在较多的H+、SO42﹣、NO3﹣,则该溶液中还可能大量存在的离子组是()
A. Al3+、CH3COO﹣、Cl﹣ B. Mg2+、Ba2+、Br﹣
C. Mg2+、Cl﹣、I﹣ D. Na+、NH4+、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
1)气体化合物A分子式可表示为OxFy,已知同温同压下10mL A受热分解生成15mL O2和10mL F2,则A的化学式为
(2)氯气与NaOH溶液吸收的离子方程式为
(3)实验室配制500ml 0.1mol•L﹣1的Na2CO3溶液,回答下列问题:
(a)应用托盘天平称取碳酸钠粉末 g.
(b)配制时应选用的仪器有500ml容量瓶,托盘天平、烧杯、药匙 .
(c)若实验时遇到下列情况,所配溶液的浓度偏大的是 .
A、加水定容时超过刻度线,又吸出少量水至刻度线;
B、忘记将洗涤液转入容量瓶;
C、容量瓶洗涤后内壁有水珠而未作干燥处理;
D、称量碳酸钠粉末时左盘放砝码,右盘放药品;
E、定容时俯视刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4mol/L,SO42﹣的物质的量浓度为0.7mol/L,则此溶液中K+的物质的量浓度为( )
|
| A. | 0.1mol/L | B. | 0.15mol/L | C. | 0.2mol/L | D. | 0.25mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分离提纯的方法正确的是()
A. 除去氯化铵中的碘,用升华的方法
B. 用酒精提取碘水中的碘
C. 分馏法分离乙醇和乙酸
D. 用重结晶法除去硝酸钾中的氯化钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com