
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题。

(1)CO可用于合成甲醇。在体积可变的密闭容器
中充入4molCO和8molH2,在催化剂作用下合成甲醇:
CO(g)+2H2(g) CH3OH(g)(Ⅰ),平衡时CO
CH3OH(g)(Ⅰ),平衡时CO
的转化率与温度、压强的关系如右图所示:
①该反应的逆反应属于________反应;(填“吸热”或
“放热”)。
②在0.1Mpa 、100℃的条件下,该反应达到平衡时容
器体积为开始容器体积的_________倍。(结果保留两位小数点)
③在温度和容积不变的情况下,再向平衡体系中充入4molCO,8molH2,达到平衡时CO转化率_______(填“增大”,“不变”或“减小”), 平衡常数K_______(填“增大”,“不变”或“减小”)。
(2)在反应(Ⅰ)中需要用到H2做反应物,以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+ H2O(g)= CO(g)+3H2(g) △H=+206.2 kJ·mol-1
CH4(g)+ CO2(g)= 2CO(g)+2H2(g) △H=+247.4 kJ·mol-1
则CH4和H2O(g)反应生成CO2和H2的热化学方程式为: 。
(3)在反应(Ⅰ)中制得的CH3OH 即可以做燃料,还可以与氧气组成碱性燃料电池,电解质溶液是20%~30%的KOH溶液。则该燃料电池放电时:负极的电极反应式为_______________________________。
科目:高中化学 来源: 题型:
汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NO2等有毒气体,其污染问题也成为当今社会急需解决的问题。
I.对汽车加装尾气净化装置,可使CO、NOx有毒气体相互反应转化为无毒气体。
2xCO+2NOx ==2xCO2+N2
当转移电子物质的量为0.8x mol时,该反应生成 LN2(标准状况下)。
II.一氧化碳是一种用途相当广泛的化工基础原料。可以还原金属氧化物,可以用来合成很多有机物如甲醇(CH3OH)、二甲醚(CH3OCH3)等,还可以作燃料。
(1)在压强为0.1 MPa条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇: CO(g)+2H2(g)  CH3OH(g) △H<0
CH3OH(g) △H<0
①该反应的平衡常数表达式为 。
②若容器容积不变,下列措施可增加甲醇产率的是 。
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1 mol CO和3 mol H2
(2)已知:①CO(g)+2H2(g) CH3OH(g) △H=-90.7 kJ·mol-1
CH3OH(g) △H=-90.7 kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H=-23.5 kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H=-41.2 kJ·mol-1
CO2(g)+H2(g) △H=-41.2 kJ·mol-1
则3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)的△H= 。
CH3OCH3(g)+CO2(g)的△H= 。
(3)CO—空气燃料电池中使用的电解质是搀杂Y2O3的ZrO2晶体,它在高温下能传导O2—。
该电池负极的电极反应式为 。
(4)甲醇也是新能源电池的燃料,但它对水质会造成一定的
 污染。有一种电化学法可消除这种污染。其原理是:2滴甲醇,1mL 1.0mol·L—1硫酸,4mL 0.1mol·L—1硫酸钴(CoSO4)混合溶液,插上两根惰性电极,通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧
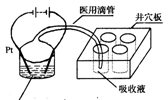
污染。有一种电化学法可消除这种污染。其原理是:2滴甲醇,1mL 1.0mol·L—1硫酸,4mL 0.1mol·L—1硫酸钴(CoSO4)混合溶液,插上两根惰性电极,通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧 化成CO2而净化。实验室用右图装置模拟上述过程:
化成CO2而净化。实验室用右图装置模拟上述过程:
①检验电解时产生的CO2气体,井穴板穴孔内应盛放 溶液。
②写出净化甲醇的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:


(1)乙中含有的官能团的名称为____________________。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

其中反应I的反应类型是_______________,反应II的条件是___________________
(3)由甲出发合成丙的路线之一如下:

①下列物质不能与B反应的是 (选填序号)。
a.金属钠 b.FeCl3 c.碳酸钠溶液 d.HBr
②丙的结构简式为 。
③写出反应③的化学方程式为
④写出D符合下列条件的所有同分异构体的结构简式 。
a.苯环上的一氯代物有两种 b.遇FeCl3溶液发生显色反应 c.能与Br2/CCl4溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,将V1 ml 0.1 mol /L NaOH溶液和V2 ml 0.1 mol /L的CH3COOH溶液充分混合,若混合后溶液呈中性,则该混合溶液中有关粒子的浓度应满足的关系是
A.c (Na+)= c (CH3COO-)+c (CH3COOH) B.c (Na+)>c (CH3COO-)
C.c (Na+) + c (H+)=c (CH3COO-) D.c (Na+)=c (CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58 g白色沉淀生成,在所得的浑浊液中,逐滴加入0.50 mol/L盐酸,加入盐酸的体积(V)与沉淀质量(W)变化关系如图所示:

(1)混合物中NaOH的质量为_________g,混合物中AlCl3的质量为___________g,混合物中MgCl2的质量为_____________g.
(2)P点表示盐酸的体积是____________mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
把7.4 g Na2CO3·10H2O 和 NaHCO3组成的混合物溶于水配成100mL溶液,其中c(Na+)=0.6mol/L。若把等质量的混合物加热至恒重,残留物的质量是
A.3.18g B.2.12g C.4.22g D.5.28g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com