
含相同原子数和价电子数的微粒互称为等电子体。如SO2是含三原子18价电子的分子,下列微粒与SO2互为等电子体的是( )
A.O3和H2S B.CO2和NO2
C.N2O+和CO2 D.O3和NO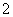
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
化合物A、B是中学常见的物质,其阴、阳离子只能从下表中选择:
| 阳离子 | K+、Na+、Fe2+、Ba2+、NH |
| 阴离子 | OH-、NO |
(1)若A、B的水溶液均为无色,且A的水溶液呈强酸性,B的水溶液呈强碱性。混合后产生不溶于稀盐酸的白色沉淀及能使湿润的红色石蕊试纸变蓝色的气体。
①B的化学式为______________。
②A、B溶液混合加热反应的离子方程式为________________________________________________________________________。
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。则
①A的化学式为______________。
②经分析上述过程中溶液变黄的原因可能有两种(用离子方程式表示)
Ⅰ________________________________________________________________________;
Ⅱ________________________________________________________________________。
③请用一简易方法证明上述溶液变黄的原因________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、NH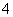 、Mg2+、Al3+、Fe3+、CO
、Mg2+、Al3+、Fe3+、CO 、SO
、SO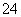 、NO
、NO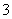 中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
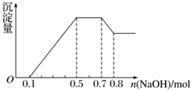
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中n(NH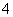 )=0.2 mol
)=0.2 mol
C.溶液中一定不含CO ,可能含有SO
,可能含有SO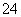 和NO
和NO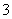
D.n(H+)∶n(Al3+)∶n(Mg2+)=2∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知五种元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期;B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子,试回答下列问题:
(1)写出五种元素的名称:
A__________,B__________,C__________,
D__________,E__________。
(2)写出A、B形成的AB型离子化合物与CO2反应的化学方程式。
(3)写出D元素形成的单质的结构式
(4)C、E元素形成化合物的空间构型为。
查看答案和解析>>
科目:高中化学 来源: 题型:
使用微波炉加热,具有使受热物质均匀、表里一致、速度快、热效率高等优点。其工作原理是通电炉内的微波场以几亿的高频改变电场的方向,水分子因而能迅速摆动,产生热效应,这是因为( )
A.水分子具有极性共价键
B.水分子中有共用电子对
C.水由氢、氧两元素组成
D.水分子是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
处于前三周期的主族元素A、B、C、D,其离子半径逐渐增大,它们的原子中核外都有一个未成对电子。已知A和D处于同一周期,0.2 mol A单质可以从D的氢化物的水溶液中置换出6.72 L H2(标准状况),试回答:
(1)写出元素符号:
A.________,B.________,C.________,D.________;
(2)若C有气态氢化物存在,比较C和D的氢化物:
沸点__________,稳定性__________,水溶液的酸性____________;
(3)四种元素的第一电离能由大到小的排列顺序是________________________;
(4)四种元素的电负性由小到大的顺序是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分被氧化的钠样品10 g,将其投入水中充分反应,将所得溶液稀释成400 mL,若实验测得该钠样品中含有8%的氧元素,则常温下所得溶液的pH为( )
A.14 B.13 C.12 D.无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com