
ŅŃÖŖ2A2(g)+B2(g) 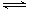 2C
2C 3(g)£»”÷H=£Q1 kJ/mol(Q1>0)£¬ ŌŚŅ»øöÓŠ“߻ƼĮµÄ¹Ģ¶ØČŻ»żµÄČŻĘ÷ÖŠ¼ÓČė2 molA2ŗĶ1 molB2£¬ŌŚ500”ꏱ³ä·Ö·“Ó¦£¬“ļĘ½ŗāŗóC3µÄÅضČĪŖw mol·L£1£¬·Å³öČČĮæĪŖQ2 kJ”£
3(g)£»”÷H=£Q1 kJ/mol(Q1>0)£¬ ŌŚŅ»øöÓŠ“߻ƼĮµÄ¹Ģ¶ØČŻ»żµÄČŻĘ÷ÖŠ¼ÓČė2 molA2ŗĶ1 molB2£¬ŌŚ500”ꏱ³ä·Ö·“Ó¦£¬“ļĘ½ŗāŗóC3µÄÅضČĪŖw mol·L£1£¬·Å³öČČĮæĪŖQ2 kJ”£
£Ø1£©“ļµ½Ę½ŗāŹ±£¬ A2µÄ×Ŗ»ÆĀŹĪŖ________”£
A2µÄ×Ŗ»ÆĀŹĪŖ________”£
£Ø2£©“ļµ½Ę½ŗāŗó£¬ČōĻņŌČŻĘ÷ÖŠĶØČėÉŁĮæµÄė²Ęų£¬A2µÄ×Ŗ»ÆĀŹ½«________£ØĢī”°Ōö“ó”°”¢”°¼õŠ””±»ņ”°²»±ä”±£©
£Ø3£©ČōŌŚŌĄ“µÄČŻĘ÷ÖŠ£¬Ö»¼ÓČė2mol C3£¬500”ꏱ³ä·Ö·“Ó¦“ļĘ½ŗāŗó£¬ĪüŹÕČČĮæQ3 kJ£¬C3ÅØ¶Č (Ģī>”¢=”¢<)w mol·L£1£¬Q1”¢Q2”¢Q3 Ö®¼äĀś×ćŗĪÖÖ¹ŲĻµ
Ö®¼äĀś×ćŗĪÖÖ¹ŲĻµ
£Ø4£©ÄÜĖµĆ÷øĆ·“Ó¦ŅŃ¾“ļµ½Ę½ŗāדĢ¬µÄŹĒ ”£
a£®v(C3)=2 v (B2)£» b£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä 
 c£®2vÄę(A2)=vÕż(B2) d£®ČŻĘ÷ÄŚµÄĆܶȱ£³Ö²»±ä
c£®2vÄę(A2)=vÕż(B2) d£®ČŻĘ÷ÄŚµÄĆܶȱ£³Ö²»±ä
£Ø5£©øıäijŅ»Ģõ¼ž£¬µĆµ½ČēĶ¼µÄ±ä»Æ¹ęĀÉ £ØĶ¼ÖŠT±ķŹ¾ĪĀ¶Č£¬n±ķŹ¾ĪļÖŹµÄĮ棩£¬æÉµĆ³öµÄ½įĀŪÕżČ·µÄŹĒ £»
£ØĶ¼ÖŠT±ķŹ¾ĪĀ¶Č£¬n±ķŹ¾ĪļÖŹµÄĮ棩£¬æÉµĆ³öµÄ½įĀŪÕżČ·µÄŹĒ £»
a£®·“Ó¦ĖŁĀŹc£¾b£¾a
b£®“ļµ½Ę½ŗāŹ±A2µÄ×Ŗ»ÆĀŹ“óŠ”ĪŖ£ŗb£¾a£¾c
c£®T2£¾T1
d. bµćA2ŗĶB2µÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ1
£Ø6£©Čō½«ÉĻŹöČŻĘ÷øÄĪŖŗćŃ¹ČŻĘ÷(·“Ó¦Ē°Ģå»żĻąĶ¬)£¬Ęš Ź¼Ź±¼ÓČė2 molA2ŗĶl molB2£¬500”ꏱ³ä·Ö·“Ó¦“ļĘ½ŗāŗ󣬷ųöČČĮæQ4 kJ£¬ŌņQ2 Q4 £ØĢī”°>”±”¢”°<”±»ņ”°=”±£©”£
Ź¼Ź±¼ÓČė2 molA2ŗĶl molB2£¬500”ꏱ³ä·Ö·“Ó¦“ļĘ½ŗāŗ󣬷ųöČČĮæQ4 kJ£¬ŌņQ2 Q4 £ØĢī”°>”±”¢”°<”±»ņ”°=”±£©”£
£Ø7£©ĻĀĮŠ“ėŹ©æÉŅŌĶ¬Ź±Ģįøß·“Ó¦ĖŁĀŹŗĶB2µÄ×Ŗ»ÆĀŹŹĒ£ØĢīŃ”ĻīŠņŗÅ£© ”£
a£®Ń”ŌńŹŹµ±µÄ“߻ƼĮ b £®Ōö“óŃ¹Ēæ c£®¼°Ź±·ÖĄėÉś³ÉµÄC3 d£®ÉżøßĪĀ¶Č
£®Ōö“óŃ¹Ēæ c£®¼°Ź±·ÖĄėÉś³ÉµÄC3 d£®ÉżøßĪĀ¶Č
 ŗ®¼ŁĄÖŌ°±±¾©½ĢÓż³ö°ęÉēĻµĮŠ“š°ø
ŗ®¼ŁĄÖŌ°±±¾©½ĢÓż³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŗģĮ×(P)ŗĶCl2·¢Éś·“Ӧɜ³ÉPCl3ŗĶPCl5£¬·“Ó¦¹ż³ĢŗĶÄÜĮæµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£¬Ķ¼ÖŠµÄ¦¤H±ķŹ¾Éś³É1 mol²śĪļµÄŹż¾Ż”£ŅŃÖŖPCl5·Ö½āÉś³ÉPCl3ŗĶCl2£¬øĆ·Ö½ā·“Ó¦ŹĒæÉÄę·“Ó¦”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
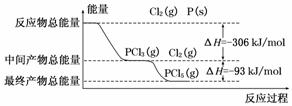
A£®ĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶ČÓŠĄūÓŚPCl5µÄÉś³É
B£®·“Ó¦2P(s)£«5Cl2(g)===2PCl5(g)¶ŌÓ¦µÄ·“Ó¦ČČ””¦¤H£½£798 kJ/mol
C£®PŗĶCl2·“Ӧɜ³ÉPCl3µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ2P(s)£«3Cl2(g)===2PCl3(g)””¦¤H£½£306 kJ/mol
D£®ĘäĖūĢõ¼ž²»±ä£¬¶ŌÓŚ2PCl5(g)===2P(s)£«5Cl2(g)””¦¤H·“Ó¦£¬Ōö“óŃ¹Ē棬PCl5µÄ×Ŗ»ÆĀŹ¼õŠ”£¬¦¤H¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
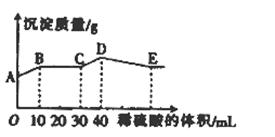
½«ÓÉNaOH”¢BaCl2”¢Al2(SO4)3ČżÖÖ¹ĢĢå×é³ÉµÄ»ģŗĻĪļČÜÓŚ×ćĮæµÄĖ®ÖŠ£¬³ä·ÖČܽā£¬Ļņ»ģŗĻĪļŅŗÖŠµĪ¼Ó1mol•L-1µÄĻ”ĮņĖį£¬¼ÓČėĻ”ĮņĖįµÄĢå»żÓėÉś³É³ĮµķµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£®ĻĀĮŠÓŠ¹ŲÅŠ¶Ļ²»ÕżČ·µÄŹĒ£Ø””””£©
A£®AB¶Ī·¢Éś·“Ó¦µÄµÄĄė×Ó·½³ĢŹ½ĪŖ£ŗBa2++2OH-+2H++SO42-=BaSO4”ż+2H2O
B£®BC¶Ī·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗH++OH-=H2O
C£®Dµć±ķŹ¾µÄ³ĮµķµÄ»ÆѧŹ½ĪŖAl(OH)3”¢BaSO4
D£®Eµć±ķŹ¾µÄČÜŅŗ³ŹÖŠŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŗćĪĀŹ±£¬ŌŚŅ»¹Ģ¶ØČŻ»żµÄČŻĘ÷ÄŚ·¢ÉśČēĻĀ·“Ó¦£ŗ2NO2(g) N2O4(g)”£“ļµ½Ę½ŗāŹ±£¬ŌŁĻņČŻĘ÷ÄŚĶØČėŅ»¶ØĮæµÄNO2(g)£¬ÖŲŠĀ“ļµ½Ę½ŗāŗó£¬ÓėµŚŅ»“ĪĘ½ŗāĻą±Č£¬NO2µÄĢå»ż·ÖŹż( )
N2O4(g)”£“ļµ½Ę½ŗāŹ±£¬ŌŁĻņČŻĘ÷ÄŚĶØČėŅ»¶ØĮæµÄNO2(g)£¬ÖŲŠĀ“ļµ½Ę½ŗāŗó£¬ÓėµŚŅ»“ĪĘ½ŗāĻą±Č£¬NO2µÄĢå»ż·ÖŹż( )
A£®²»±ä B£®Ōö“ó C£®¼õŠ” D£®ĪŽ·ØÅŠ¶Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŌĻĀĪļÖŹ£»¢Ł ¼×Ķ飻¢Ś ±½£»¢Ū ¾ŪŅŅĻ©£»¢Ü ¾ŪŅŅČ²£»¢Ż 2-¶”Č²£»¢Ž »·¼ŗĶ飻¢ß ĮŚ¶ž¼×±½£»¢ą ±½ŅŅĻ©”£¼ČÄÜŹ¹KMnO4ĖįŠŌČÜŅŗĶŹÉ«£¬ÓÖÄÜŹ¹äåĖ®Ņņ·¢Éś»Æѧ·“Ó¦¶ųĶŹÉ«µÄŹĒ£Ø £©
A£®¢Ū¢Ü¢Ż¢ą B£®¢Ü¢Ż¢ß¢ą C£®¢Ü¢Ż¢ą D£®¢Ū¢Ü¢Ż¢ß¢ą
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«AlCl3”¢FeCl2”¢FeCl3”¢MgCl2ĖÄÖÖČÜŅŗ£¬Ö»ÓĆŅ»ÖÖŹŌ¼Į¾ĶÄܼÓŅŌĒų±š£¬ÕāÖÖŹŌ¼ĮŹĒ
A£®HCl B£®NaOH C£®BaCl2 D£®KSCN
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijŠ£»ÆѧæĪĶāŠ”×éĪŖĮĖ¼ų±šĢ¼ĖįÄĘŗĶĢ¼ĖįĒāÄĘĮ½ÖÖ°×É«¹ĢĢ壬ÓĆ²»Ķ¬µÄ·½·Ø×öĮĖŅŌĻĀŹµŃ飬ČēĶ¼ÖŠ¢ń”«¢ōĖłŹ¾”£
£Ø1£©Ö»øł¾ŻĶ¼¢ń”¢¢ņĖłŹ¾ŹµŃ飬Äܹ»“ļµ½ŹµŃéÄæµÄµÄŹĒ(Ģī×°ÖĆŠņŗÅ)____ ”ų____”£
£Ø2£©Ķ¼¢ó”¢¢ōĖłŹ¾ŹµŃé¾łÄܼų±šÕāĮ½ÖÖĪļÖŹ£¬Ęä·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_________”ų__________”£
ÓėŹµŃé¢óĻą±Č£¬ŹµŃé¢ōµÄÓŵćŹĒ(ĢīŃ”ĻīŠņŗÅ)___ ”ų____£»
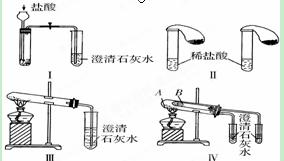 A£®¢ō±Č¢óø“ŌÓ B£®¢ō±Č¢ó°²Č«
A£®¢ō±Č¢óø“ŌÓ B£®¢ō±Č¢ó°²Č«
C£®¢ōæÉŅŌ×öµ½ÓĆŅ»Ģ××°ÖĆĶ¬Ź±½ųŠŠĮ½øö¶Ō±ČŹµŃ飬¶ų¢ó²»ŠŠ
£Ø3£©ČōÓĆŹµŃé¢ōŃéÖ¤Ģ¼ĖįÄĘŗĶĢ¼ĖįĒāÄʵÄĪČ¶ØŠŌ£¬
ŌņŹŌ¹ÜA֊װČėµÄ¹ĢĢå×īŗĆŹĒ(Ģī»Æѧ
Ź½)___ ”ų_____”£
£Ø4£©½«Ģ¼ĖįĒāÄĘČÜŅŗÓė³ĪĒåŹÆ»ŅĖ®»ģŗĻ²¢³ä·Ö·“Ó¦”£
¢Łµ±ŹÆ»ŅĖ®¹żĮæŹ±£¬ĘäĄė×Ó·½³ĢŹ½
ĪŖ___________”ų______________£»
¢Śµ±Ģ¼ĖįĒāÄĘÓėĒāŃõ»ÆøĘĪļÖŹµÄĮæÖ®
±ČĪŖ2:1Ź±£¬ĖłµĆČÜŅŗÖŠČÜÖŹµÄ»ÆѧŹ½
ĪŖ___”ų___£¬ĒėÉč¼ĘŹµŃé¼ģŃéĖłµĆČÜŅŗÖŠČÜÖŹµÄŅõĄė×Ó_____”ų______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖ2SO2(g)£«O2(g)2SO3(g)””¦¤H£½£a kJ”¤mol£1(a>0)”£ŗćĪĀŗćČŻĻĀ£¬ŌŚ10 LµÄĆܱÕČŻĘ÷ÖŠ¼ÓČė0.1 mol SO2ŗĶ0.05 mol O2£¬¾¹ż2 min“ļµ½Ę½ŗāדĢ¬£¬·“Ó¦·ÅČČ0.025 a kJ”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ(””””)
A£®ŌŚ2 minÄŚ£¬v(SO2)£½0.0025 mol”¤L£1”¤min£1
B£®ČōŌŁ³äČė0.1 mol SO3£¬“ļµ½Ę½ŗāŗóSO3µÄÖŹĮæ·ÖŹż»į¼õŠ”
C£®ŌŚ1 minŹ±£¬c(SO2)£«c(SO3)£½0.01 mol”¤L£1
D£®ČōŗćĪĀŗćŃ¹ĻĀ£¬ŌŚ10 LµÄĆܱÕČŻĘ÷ÖŠ¼ÓČė0.1 mol SO2ŗĶ0.05 mol O2£¬Ę½ŗāŗó·“Ó¦·ÅČČŠ”ÓŚ0.025a kJ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com