
 2SO3��g�� ��H����196kJ��mol��
2SO3��g�� ��H����196kJ��mol��
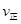 _______
_______
| A����1����2��1 | B��Q1��Q2��196 |
| C����3<��1 | D��P3��2P1��2P2 |
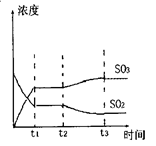
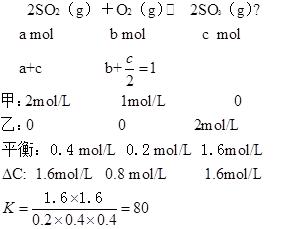
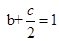
 ��ƽ�������ƶ���
��ƽ�������ƶ���


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO2(g)+H2(g)��CO2(g)��ƽ�����ʵ���Ũ��c(CO2)���¶�T�Ĺ�ϵ��ͼ��ʾ������˵���������
CO2(g)+H2(g)��CO2(g)��ƽ�����ʵ���Ũ��c(CO2)���¶�T�Ĺ�ϵ��ͼ��ʾ������˵���������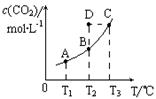
A����ӦCO(g)+H2O(g) CO2(g)+H2(g)����H >0 CO2(g)+H2(g)����H >0 |
| B����T2ʱ������Ӧ���е�״̬D����һ����v������<v���棩 |
| C����ʹD״̬��ΪC״̬�����Բ�ȡ����������T3�ķ�ʽ |
| D����T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1<K2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 PH3��g�� + HI��g�� �� ��
PH3��g�� + HI��g�� �� ��  P4��g��+ 6 H2��g�� �� ��
P4��g��+ 6 H2��g�� �� �� H2��g�� + I2��g�� ��
H2��g�� + I2��g�� ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2Z��g�� ��H����a kJ��mol��1��a��0������һ���ݻ��̶��������м���2molX2��1mo1Y2����500��Գ�ַ�Ӧ��ƽ���Z��Ũ��ΪW mol��L��1���ų�����b kJ��
2Z��g�� ��H����a kJ��mol��1��a��0������һ���ݻ��̶��������м���2molX2��1mo1Y2����500��Գ�ַ�Ӧ��ƽ���Z��Ũ��ΪW mol��L��1���ų�����b kJ��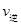 ��X2����2
��X2����2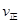 ��Y2�� d�������ڵ��ܶȱ��ֲ���
��Y2�� d�������ڵ��ܶȱ��ֲ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
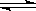 B(?)+ 2C(?) ��H��0��������ͼ��ʾ�Ĺ�ϵ��������˵������ȷ����
B(?)+ 2C(?) ��H��0��������ͼ��ʾ�Ĺ�ϵ��������˵������ȷ���� 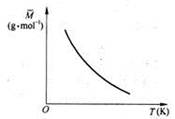
| A��B��C���ܾ�Ϊ����̬ |
| B����B����̬����Cһ��Ҳֻ������̬ |
| C����BΪ��̬����Cһ��Ϊ��̬ |
| D��B��C���ܾ�����̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g)������ӦΪ���ȷ�Ӧ����Ϊ��ʹƽ��������Z�ķ����ƶ���Ӧѡ�����е����������ǣ� ��
2Z(g)������ӦΪ���ȷ�Ӧ����Ϊ��ʹƽ��������Z�ķ����ƶ���Ӧѡ�����е����������ǣ� ��| A���٢ܢ� | B���ڢۢ� | C���٢ۢ� | D���ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
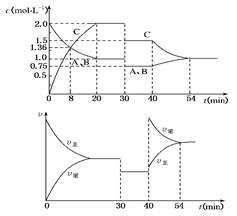
| A��30 minʱ�����¶ȣ�40 minʱ�����¶� |
| B�� 0��8 min��A��ƽ����Ӧ����Ϊ0.08 mol��L��1��min��1 |
| C����Ӧ����ʽ�е�x��1������ӦΪ���ȷ�Ӧ |
| D�� 54 minʱC�������������40 minʱ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ơ��ƿ��ƿ�����̷��������ĭ |
| B����H2��I2������HI��ɵ�ƽ����ϵ��ѹ����ɫ���� |
| C���ں���Fe��SCN��3�ĺ�ɫ��Һ�м������ۣ����ã� |
| D����ˮӦ�ܱձ��棬�õ��´� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ������Ӧ�ﵽƽ��ʱ��CO���������Ϊx����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO�������������x����(����)
������Ӧ�ﵽƽ��ʱ��CO���������Ϊx����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO�������������x����(����)| A��0.5 mol CO��2 mol H2O(g)��1 mol CO2��1 mol H2 |
| B��1 mol CO��1 mol H2O(g)��1 mol CO2��1 mol H2 |
| C��0.5 mol CO��1.5 mol H2O(g)��0.4 mol CO2��0.4 mol H2 |
| D��0.5 mol CO��1.5 mol H2O(g)��0.5 mol CO2��0.5 mol H2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com