
【题目】部分弱酸的电离平衡常数如表:

(1)上表的6种酸进行比较,酸性最弱的是:_____;HCOO-、S2-、HSO3-三种离子中,最难结合H+的是__________。
(2)在浓度均为0.1mol/L的HCOOH和H2C2O4混合溶液中,逐渐滴入0.1mol/L的NaOH溶液,被OH-先后消耗的酸及酸式酸根依次是:_________。
(3)已知HNO2具有强氧化性,弱还原性。将HNO2溶液滴加到H2S溶液中,同时有沉淀和无色气体生成,该气体遇空气立即变为红棕色,试写出两酸之间的化学反应方程式:___。
(4)下列离子方程式书写正确的是________。
A.HNO2+HS-=NO2-+H2S↑
B.2HCOOH+SO32-=2HCOO-+H2O+SO2↑
C.H2SO3+2HCOO-=2HCOOH+SO32-
D.H2SO3+SO32-=2HSO3-
E.H2C2O4+NO2-=HC2O4-+HNO2
(5)将少量的SO2通入Na2C2O4溶液,写出离子方程式___。
(6)已知HX为一元弱酸。HX的电离常数为5.5×10﹣8。某混合溶液中含有4molNaX、2molNa2CO3和1molNaHCO3。往溶液中通入3molCO2气体,充分反应后,气体全部被吸收,计算某些物质的量:Na2CO3______、NaHCO3______。
【答案】H2S HSO3﹣ H2C2O4、HCOOH、HC2O4﹣ 2HNO2+H2S=2H2O+2NO↑+S↓ DE SO2+H2O+C2O42-=HC2O4-+HSO3﹣ 0mol 6mol
【解析】
(1)相同温度下,酸的电离平衡常数越小,其酸性越弱,弱酸的酸性越强,其酸根离子水解程度越小,则结合氢离子能力越弱;
(2)酸的电离平衡常数越大,该酸的酸性越强,与碱反应越容易,根据酸的电离平衡常数大小判断;
(3)HNO2和H2S发生氧化还原反应,生成沉淀和无色气体,无色气体遇空气立即变为红棕色,则该无色气体是NO,亚硝酸具有强氧化性,硫化氢具有还原性,所以硫化氢被亚硝酸氧化生成S单质,根据元素守恒知还生成水,据此书写方程式;
(4)强酸能和弱酸的盐反应生成弱酸和强酸盐;
(5)将少量的SO2通入Na2C2O4溶液,酸性H2C2O4>H2SO3>HC2O4->HSO3-,据此写出离子方程式;
(6)已知HX为一元弱酸,某混合溶液中含有4mol NaX、2mol Na2CO3和1molNaHCO3,NaX、NaHCO3能共存,说明HX的酸性强于碳酸氢根离子,往溶液中通入3mol
CO2气体,充分反应后,气体全部被吸收,说明HX的酸性弱于碳酸,即溶液中除了发生Na2CO3+CO2+H2O=2NaHCO3,还发生反应NaX+CO2+H2O=HX+NaHCO3,根据反应方程式进行计算。
(1)相同温度下,酸的电离平衡常数越小,其酸性越弱,弱酸的酸性越强,其酸根离子水解程度越小,则结合氢离子能力越弱,根据电离平衡常数知,酸性最弱的是H2S,酸性最强的是H2SO3,所以结合氢离子能力最弱的是HSO3-;
(2)酸的电离平衡常数越大,该酸的酸性越强,与碱反应越容易,根据酸的电离平衡常数知,被OH﹣先后消耗的酸及酸式酸根依次是H2C2O4、HCOOH、HC2O4-;
(3)HNO2和H2S生成沉淀和无色气体,无色气体遇空气立即变为红棕色,则该无色气体是NO,亚硝酸具有强氧化性,硫化氢具有还原性,所以硫化氢被亚硝酸氧化生成S单质,根据元素守恒知还生成水,该反应方程式为2HNO2+H2S=2H2O+2NO↑+S↓;
(4)A.HNO2具有强氧化性,HS-具有还原性,二者能发生氧化还原反应,根据电子守恒、电荷守恒、离子守恒,可得反应的离子方程式为H++2HNO2+HS-=2NO↑+S↓+2H2O,A错误;
B.酸性:H2SO3>HCOOH>HSO3-,所以HCOOH和SO32-反应生成HCOO-和HSO3-,反应的离子方程式为HCOOH+SO32-=HCOO-+HSO3-,B错误;
C.酸性:H2SO3>HCOOH>HSO3-,所以H2SO3和HCOO-反应生成HCOOH、HSO3-,反应的离子方程式为H2SO3+HCOO-=HCOOH+HSO3-,C错误;
D.亚硫酸和亚硫酸根离子反应生成亚硫酸氢根离子,离子方程式为H2SO3+SO32-=2HSO3-,D正确;
E.根据电离平衡常数可知,H2C2O4的一级电离平衡常数大于HNO2,二级电离平衡常数小于HNO2,所以H2C2O4+NO2-=HC2O4-+HNO2,E正确;
故合理选项是DE;
(5)将少量的SO2通入Na2C2O4溶液,酸性H2C2O4>H2SO3>HC2O4->HSO3-,据此离子方程式为:SO2+H2O+C2O42-=HC2O4-+HSO3-;
(6)已知HX为一元弱酸,某混合溶液中含有4molNaX、2molNa2CO3和1molNaHCO3,NaX、NaHCO3能共存,说明HX的酸性强于HCO3-,往溶液中通入3molCO2气体,充分反应后,气体全部被吸收,说明HX的酸性弱于H2CO3,溶液中发生的反应有:Na2CO3+CO2+H2O=2NaHCO3,根据该反应可知2molNa2CO3能生成4molNaHCO3同时消耗二氧碳2molCO2,还有1molCO2发生反应NaX+CO2+H2O=HX+NaHCO3,生成1molNaHCO3,所以溶液中没有Na2CO3,Na2CO3的物质的量是0,NaHCO3的物质的量为1mol+4mol+1mol=6mol。


科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择__________(填字母)。
a.碳棒b.锌板c.铜板

(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的________(填“正”或“负”)极。F电极上的电极反应式为____________________________________________________________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_________________________________________________________________________。

(3)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图3所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为_______________________________________________________。
②若有2mol H+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯和溴的取代反应的实验装置如图所示,其中A为带支管口的试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉。填写下列空白:
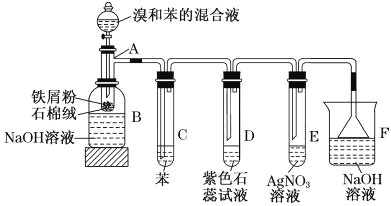
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):_____;
(2)试管C中苯的作用是_____,反应开始后,观察D和E两试管,D中看到的现象为____,E中发生的反应为(写离子方程式)______。
(3)反应2min~3min后,在B中可观察到的现象是______,B中NaOH溶液的作用是:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分支酸用于生化研究,可以由物质A合成.已知:连4个不相同的原子或原子团的碳原子是手性碳原子.
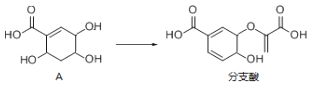
下列叙述不正确的是![]()
A.用![]() 溶液可鉴别化合物A和分支酸
溶液可鉴别化合物A和分支酸
B.化合物A中含有3个手性碳原子
C.1mol分支酸在一定条件下最多可与![]() 发生反应
发生反应
D.在浓硫酸和加热条件下,化合物A可发生消去反应生成多种有机产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁均为中学化学常见物质,一定条件下它们有如下转化关系![]() 其它产物已略去
其它产物已略去![]() 。
。
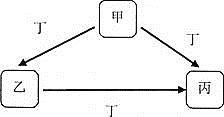
![]() 若丁为KOH溶液,写出乙的一种用途________,甲
若丁为KOH溶液,写出乙的一种用途________,甲![]() 丙的离子方程式为________。
丙的离子方程式为________。
![]() 若丁为Fe,写出向丙溶液中加入NaOH溶液的化学方程式:________;该实验现象为________。
若丁为Fe,写出向丙溶液中加入NaOH溶液的化学方程式:________;该实验现象为________。
![]() 若甲、乙、丙均为焰色反应呈黄色的化合物,则丁可能为________。
若甲、乙、丙均为焰色反应呈黄色的化合物,则丁可能为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是A、B两种重要的有机合成原料的结构。下列有关说法中正确的是
A. ![]() B.
B.![]()
A.A与B互为同系物
B.A与B都能与溴的四氯化碳溶液发生加成反应
C.在一定条件下,A与B均能发生取代反应
D.1mol B能与4mol![]() 发生加成反应
发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是( )
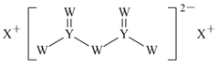
A.熔点:Y单质高于X单质
B.元素非金属性强弱的顺序为W>Y>Z
C.W的简单氢化物稳定性比Y的简单氢化物稳定性低
D.W分别与X、Y、Z形成的二元化合物均只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在10 mL0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/LHCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未两出,忽略因气体逸出引起的溶液体积变化),下列说法不正确的是( )
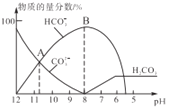
A.Kw(CO32-)的数量级为10-4
B.当溶液是中性时,溶液的总体积大于20 mL
C.在0.1 mol/L Na2CO3溶液中:c(OH-)>c(H2CO3)+c(HCO3-)+c(H+)
D.在B点所示的溶液中离子浓度最大的是HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有如下三个热化学方程式
H2(g)+ ![]() O2(g)=H2O(g) ΔH1=a kJ·mol-1
O2(g)=H2O(g) ΔH1=a kJ·mol-1
H2(g)+ ![]() O2(g)=H2O(l) ΔH2=b kJ·mol-1
O2(g)=H2O(l) ΔH2=b kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH3=c kJ·mol-1
关于它们的下列表述正确的是( )
A.它们都是吸热反应B.a、b、c均为正值C.a=bD.2b=c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com