
【题目】![]() 时,用浓度为
时,用浓度为![]() 的氢氧化钠溶液分别滴定
的氢氧化钠溶液分别滴定![]() 浓度均为
浓度均为![]() 的二种酸HX、
的二种酸HX、![]() 忽略体积变化
忽略体积变化![]() ,实验数据如下表,下列判断正确的是
,实验数据如下表,下列判断正确的是![]()
数据编号 | NaOH加入的体积 | 溶液的pH | |
|
| ||
① | 0 | 3 | 1 |
② | a | 7 | |
③ |
| x | y |
A.在相同温度下,同浓度的两种酸溶液的导电能力顺序![]()
B.由表中数据可估算出![]()
C.HY和HX混合,![]()
D.上述②反应后的HY溶液中:![]()
【答案】A
【解析】
A.根据表中数据分析,![]() 的酸HX、HY的pH分别为3、1,可知HX为弱酸、HY为强酸,同浓度的两种酸溶液的导电能力顺序
的酸HX、HY的pH分别为3、1,可知HX为弱酸、HY为强酸,同浓度的两种酸溶液的导电能力顺序![]() ;
;
B.HY为强酸,不存在电离平衡常数;
C.根据混合液中的物料守恒和电荷守恒分析;
D.HY为强酸,与氢氧化钠反应时HY酸过量,溶液显酸性,![]() 。
。
A.由①知,![]() 的HY溶液的
的HY溶液的![]() ,说明HY是强酸;而
,说明HY是强酸;而![]() 的HX溶液的
的HX溶液的![]() ,说明HX是弱酸,所以在相同温度下,同浓度的两种酸溶液的导电能力顺序
,说明HX是弱酸,所以在相同温度下,同浓度的两种酸溶液的导电能力顺序![]() ,故A正确;
,故A正确;
B.根据分析可知,HY为强酸,则不存在电离平衡常数,故B错误;
C.将![]() 的HX和HY混合,当达平衡时,根据物料守恒得①
的HX和HY混合,当达平衡时,根据物料守恒得①![]() ,将①代入到电荷守恒
,将①代入到电荷守恒![]() 中可得:
中可得:![]() ,故C错误;
,故C错误;
D.上述②反应后的HX溶液显中性,因为HX为弱酸,则![]() mL,由于HY为强酸,故HY酸过量,
mL,由于HY为强酸,故HY酸过量,![]() ,结合电荷守恒可知:
,结合电荷守恒可知:![]() ,溶液中正确的离子浓度大小为:
,溶液中正确的离子浓度大小为:![]() ,故D错误;
,故D错误;
故答案选A。


 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】氮元素可形成很多重要的化合物,其中叠氮化钠(NaN3)被广泛应用于汽车安全气囊。叠氮化钠的制取方法是:①金属钠与液态氨反应得NaNH2②NaNH2与N2O按物质的量2:1反应可生成NaN3、NaOH和一种气体。
(1)请写出反应②的化学方程式为:____________。
(2)与N3-互为等电子体的分子有:______(写一种)由此可推知N3-的空间构型是:_________; 比较NH2-和NH3的键角∠HNH的大小:NH2- ____ NH3(填“>”或“<”或“=”),请用价层电子对互斥规律解释_______。
(3)叠氮化钠(NaN3)分解可得纯N2,有关说法正确的是:________(选填代号)
A.氮气常温下很稳定,是因为氮元素的电负性大
B.NaN3与KN3结构类似,前者晶格能较小
C.第一电离能(I1):N>P>S
D.热稳定性NH3强于PH3和H2S是因为NH3分子间有氢键
(4)小汽车的防撞气囊中叠氮化钠的工作原理是基于反应:6NaN3+ Fe2O3 = 3Na2O + 2Fe+ 9N2 ;铁晶体有三种堆积方式,其中两种堆积方式分别如图甲、图乙所示(其晶胞特征如下图所示):
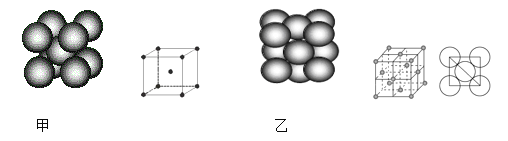
晶胞甲中铁原子的配位数为:_______,晶胞乙中铁原子的堆积方式为:________。晶胞乙中铁原子半径为a cm,NA表示阿伏加德罗常数,摩尔质量为M g/mol。则该晶体的密度可表示为:___________ g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属锰及化合物广泛应用于工业生产、制造业等领域。
(1)科研人员将锰粉碎后加入到![]() 溶液中使其浸出(假定杂质不反应,溶液体积不变),发生反应
溶液中使其浸出(假定杂质不反应,溶液体积不变),发生反应![]() (已知含
(已知含![]() 水溶液为米黄色)
水溶液为米黄色)
①为加快上述反应速率可以采取的措施有________(写出一条即可)。不考虑温度因素,一段时间后Mn的溶解速率加快,可能的原因是_______。
②下列说明反应已达平衡的有_______(填编号)。
A.溶液的颜色不发生变化
B.溶液中![]()
C.体系中固体的质量不变
D.![]() 与
与![]() 浓度的比值保持不变
浓度的比值保持不变
③室温下,测得溶液中阳离子浓度![]() 随时间的变化情况如下图所示,则上述反应的平衡常数K=___,
随时间的变化情况如下图所示,则上述反应的平衡常数K=___,![]() 的转化率为_____。
的转化率为_____。
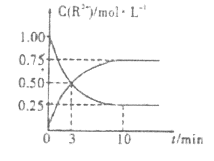
④若其他条件不变,10mim后向容器中迅速加入蒸馏水至溶液体积变为原来的2倍,则再次平衡时![]() =_____(不考虑离子水解的影响)。
=_____(不考虑离子水解的影响)。
(2)![]() 也可在
也可在![]() 为体系的电解液中电解获得,其阳极反应式为_____。
为体系的电解液中电解获得,其阳极反应式为_____。
(3)电解制锰后的废水中含有![]() ,常用石灰乳进行一级沉降得到
,常用石灰乳进行一级沉降得到![]() 沉淀,过滤后再向滤液中加入等体积的
沉淀,过滤后再向滤液中加入等体积的![]() 溶液,进行二级沉降,为了将
溶液,进行二级沉降,为了将![]() 的浓度降到
的浓度降到![]() ,则加入的
,则加入的![]() 溶液的浓度至少是___mol/L[已知
溶液的浓度至少是___mol/L[已知![]() ]。
]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应:mA(g)+nB(g)![]() r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是
r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是

A. T1>T2,p1>p2,m+n>r,正反应吸热
B. T1<T2,p1<p2,m+n<r,正反应吸热
C. T1>T2,p1>p2,m+n<r,正反应放热
D. T1<T2,p1<p2,m+n>r,正反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钠晶体 ![]() 俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿
俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿![]() 主要成份为
主要成份为![]() ,还含有
,还含有![]() 、MgO、
、MgO、![]() 等杂质
等杂质![]() 为主要原料进行生产,其主要工艺流程如下:
为主要原料进行生产,其主要工艺流程如下:
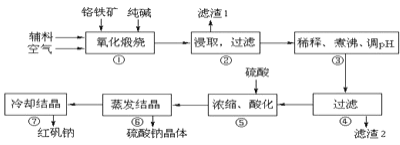
①中涉及的主要反应有:
主反应:![]()
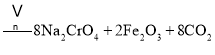
副反应: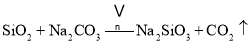 、
、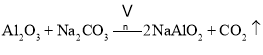
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
沉淀物 |
|
|
|
|
完全沉淀时溶液pH |
|
|
|
|
试回答下列问题:/span>
![]() “①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是 ______
“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是 ______
![]() “③”中调节pH至
“③”中调节pH至![]() ,目的是 ______ .
,目的是 ______ .
![]() “⑤”中加硫酸酸化的目的是使
“⑤”中加硫酸酸化的目的是使![]() 转化为
转化为![]() ,请写出该平衡转化的离子方程式: ______ .
,请写出该平衡转化的离子方程式: ______ .
![]() 称取重铬酸钠试样
称取重铬酸钠试样![]() 配成250mL溶液,取出
配成250mL溶液,取出![]() 于碘量瓶中,加入10mL
于碘量瓶中,加入10mL![]() 和足量碘化钠
和足量碘化钠![]() 铬的还原产物为
铬的还原产物为![]() ,放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用
,放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用![]() 标准溶液滴定
标准溶液滴定![]()
①判断达到滴定终点的依据是: ______ ;
②若实验中共用去![]() 标准溶液
标准溶液![]() ,所得产品的中重铬酸钠晶体的纯度
,所得产品的中重铬酸钠晶体的纯度![]() 设整个过程中其它杂质不参与反应
设整个过程中其它杂质不参与反应![]() ______ .
______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,可逆反应C(s)+CO2(g)![]() 2CO(g),达到平衡状态的标志是( )
2CO(g),达到平衡状态的标志是( )
①单位时间内生成n molCO2的同时生成n molC ②单位时间内生成n molCO2 的同时生成2n mol CO ③CO2 、CO的物质的量浓度之比为1: 2的状态 ④混合气体的密度不再改变的状态 ⑤混合气体的压强不再改变的状态 ⑥C的质量不再改变的状态
A. ①④⑤⑥ B. ②④⑤⑥ C. ②③⑤⑥ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.溴乙烷与少量乙醇的混合物加水除去乙醇的方法,原理类似于溴水中加四氯化碳萃取溴
B.中和滴定实验中,如用于盛放待测溶液的锥形瓶洗净后未干燥,不影响测定结果
C.由![]() 稀
稀![]() 构成的原电池,溶液中加入适量
构成的原电池,溶液中加入适量![]() 能提高电池放电效率
能提高电池放电效率
D.蛋白质与氨基酸遇到双缩脲试剂均会出现紫玫瑰色现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Q、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4,M原子的最外层电子数与次外层电子数之比为3∶4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,Q和Y在周期表中的位置相邻。请回答下列问题。
(1)M原子的价电子排布图是__________,Q的常见氢化物的立体构型是_________________。
(2)写出X、Y、R按原子个数之比1∶1∶1形成的化合物的结构式:_______________。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:_________。
(4)写出单质R的一种工业用途:_______________。
(5)图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式:_______。

(6)由X、Y、Z、M四种元素可形成一种离子化合物A,已知A既能与盐酸反应,又能与氢氧化钠溶液反应,还能和氯水反应,写出A与氯水反应的离子方程式:_____。
(7)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是自来水表的常见安装方式。下列有关说法不正确的是( )

A. 发生腐蚀过程中,电子从接头流向水表
B. 腐蚀时,铁接头发生的是还原反应
C. 腐蚀时铜质水表发生的电极反应为:2H2O+O2+4e—=4OH—
D. 腐蚀过程还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com