
一定条件下,在体积为10 L的固定容器中发生反应:
N2(g)+3H2(g)  2NH3(g) ΔH<0,反应过程如图:
2NH3(g) ΔH<0,反应过程如图:
下列说法正确的是
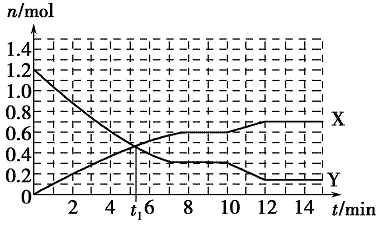
A.t1 min时正、逆反应速率相等
B.X曲线表示NH3的物质的量随时间变化的关系
C.0~8 min,H2的平均反应速率v(H2)=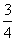 mol·L-1·min-1
mol·L-1·min-1
D.10~12 min,升高温度使反应速率加快,平衡正向移动
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
请回答:
(1)这九种元素分别是(填元素符号)① 、② 、③ 、④ 、⑤ 、⑥ 、⑦ 、⑧ 、⑨ ,其中化学性质最不活泼的是 。
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是 (填化学式)。
(3)①、②、③三种元素按原子半径由大到小的顺序依次为 (填元素符号)。
(4)⑥元素的氢化物是 (填化学式),该氢化物在常温下与②发生反应的离子方程式为 ,所得溶液的pH (填“<”、“>”或“=”)7
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A 是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
 |
请回答下列问题:
(1)写出A的结构简式 。
(2)B、D分子中的官能团名称分别是 、 。
(3)物质B可以被直接氧化为D,需要加入的试剂是 。
(4)写出下列反应的化学方程式:
① ;反应类型: 。
④ ;反应类型: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.使甲基橙变红色的溶液:Mg2+、K+、SO42-、NO3-
B.使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3-
C. 水电离出的c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32-
D.能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.pH=2与pH=1的硝酸中c(H+)之比为1:10
B.H2CO3溶液中c(H+)与c(CO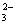 )之比为2:1
)之比为2:1
C.0.2mol/L与0.1mol/L醋酸中c(H+)之比为2:1
D.NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
在一容积为2 L的密闭容器内加入0.2 molA和0.6 molB,在一定条件下发生反应:A(s)+3B(g) 2C(s)+3D(g) 已知该反应在不同温度下的平衡常数如下表:
2C(s)+3D(g) 已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 64.0 | 50.7 | 42.9 |
请回答下列问题:
⑴该反应的平衡常数表达式K= ,ΔH 0(填“>”或“<”)。
⑵1000 ℃时,4 min后达到平衡.求B的平衡转化率为 ,平衡时B的体积分 数 。
⑶欲提高⑵中B的平衡转化率,可采取的措施是
A.减少C的量 B.增加A的量 C.移出部分D
D.降低反应温度 E.减小容器的容积 F.加入合适的催化剂
⑷1000 ℃时, 在一容积为2 L的密闭容器内加入XmolC和0.6 molD,5 min后达到平衡,B的浓度与⑵中B的浓度相同,求X的范围
⑸下列说法中能说明反应已达到平衡状态的是
A.容器内混合气体的压强不随时间变化而变 B.B的速率不随时间的变化而变化
C.c(B)︰c(D)=1︰1 D.混合气体的密度保持不变(M(B)≠M(D))
查看答案和解析>>
科目:高中化学 来源: 题型:
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,该晶体具有Na2CO3和H2O2的双重性质。利用图2装置制备过碳酸钠,在冷水浴中充分反应后,按图1流程可获得过碳酸钠产品。
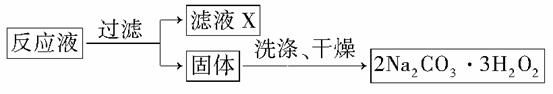
图1

(1)恒压滴液漏斗中支管的作用是________________________。
(2)制备过碳酸钠的关键是______________________________。
(3)如果配制过碳酸钠的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至完全失去杀菌作用。试分析其中的原因_____________
(写出其中一种即可,用方程式表示)。
(4)某化学学习小组为了定性探究铁离子对这种新型漂白剂的不良影响,取该漂白剂100 mL,加入25 g FeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.1 mol/L NaOH溶液、8.0 mol/L NaOH溶液、澄清石灰水、0.01 mol/L KMnO4溶液、BaCl2稀溶液、品红溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2;
假设2:气体是________________;
假设3:气体是CO2。
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象与结论。
| 实验步骤 | 预期现象与结论 |
| 将气体依次通入盛有____________的洗气瓶中,____________ | ①____________; ②____________; ③____________ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com