
| A. | 金属元素在不同的化合物中化合价均相同 | |
| B. | 所有合金都只含有金属元素 | |
| C. | 可利用铝热反应冶炼单质镁 | |
| D. | 镁合金的硬度和强度均高于纯镁 |
分析 A.金属元素中有部分变价元素,在不同的化合物中可能呈现不同的化合价;
B.合金成分不一定都是金属元素,可能含有非金属元素;
C.Mg性质比Al活泼,不能采用铝热反应冶炼Mg;
D.合金的硬度和强度都大于其任一成分.
解答 解:A.金属元素中有部分变价元素,在不同的化合物中可能呈现不同的化合价,如FeO、Fe2O3中Fe元素化合价分别是+2、+3价,故A错误;
B.合金成分不一定都是金属元素,可能含有非金属元素,如碳素钢中含有C元素,故B错误;
C.Mg性质比Al活泼,不能采用铝热反应冶炼Mg,应该用电解熔融氯化镁的熔融冶炼Mg,故C错误;
D.合金的硬度和强度都大于其任一成分,所以镁合金的硬度和强度均高于纯镁,故D正确;
故选D.
点评 本题考查金属元素化合价、合金成分及性质、金属冶炼等知识点,为高频考点,明确常见元素化合价、物质构成及其性质、金属活泼性与冶炼方法的关系是解本题关键,Na、Mg、Al等活泼金属都采用电解的方法冶炼,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 在CCl4中的溶解性Cl2<BrCl<Br2 | |
| B. | BrCl氧化性比Br2强 | |
| C. | BrCl能使润湿的淀粉碘化钾试纸变蓝 | |
| D. | 常温下BrCl可与NaOH溶液反应生成NaClO和NaBr |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
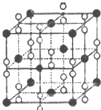 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ•mol-1) | 1681 | 1251 | 1140 | 1008 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤时如果发现滤液是浑浊的,则滤液还要进行过滤 | |
| B. | 在进行蒸馏时,要加少量碎瓷片,防止液体暴沸 | |
| C. | 在进行分液操作时,分液漏斗内外气体相通,眼睛要注视烧杯中的溶液 | |
| D. | 在进行蒸馏时,温度计不要插入溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的种类由核外电数决定 | |
| B. | 原子的种类由原子核内质子数与中子数共同决定 | |
| C. | 难失电子的原子,得电子的能力-定强 | |
| D. | 金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
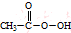 (过氧乙酸)+H2O
(过氧乙酸)+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核内有8个中子的碳原子:${\;}_{6}^{8}$C | |
| B. | Mg2+的结构示意图: | |
| C. | CO2的电子式: | |
| D. | 熔融状态下硫酸氢钾的电离方程式:KHSO4$\frac{\underline{\;熔融\;}}{\;}$K++H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉撒入稀硫酸中2Fe+6H+→2Fe3++3H2↑ | |
| B. | 向AlCl3溶液中加入过量的氨水:Al3++4NH3•H2O→AlO2-+4NH4++2H2O | |
| C. | 把金属钠放入冷水中:Na+H2O→Na++OH-+H2↑ | |
| D. | 用氢氧化钠溶液除去铝表面的氧化铝:Al2O3+2OH-→2AlO2-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 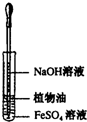 观察Fe(OH)2的生成 | B. | 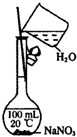 配制一定量浓度的NaNO3的溶液 | ||
| C. | 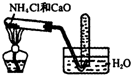 实验室制取氨气 | D. | 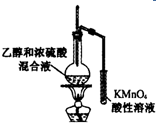 验证乙烯的生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com