
| A£® | ŌĮĻ±ćŅĖ | B£® | CO2²ĪÓėŃ»·£¬µĶĢ¼»·±£ | ||
| C£® | ²śÉśĮĖøü¶ąµÄĀČ»ÆøĘ | D£® | ŌĮĻĄūÓĆĀŹøߣ¬½ŚŹ”Éč±ø |
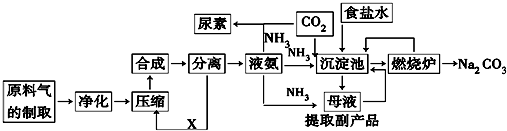
·ÖĪö Ė÷¶ūĪ¬ÖĘ¼ī·Ø¶ŌĀĖŅŗµÄ“¦ĄķŹĒ¼ÓŹģŹÆ»ŅŹ¹°±ĘųŃ»·£¬²śÉśµÄCaCl2£¬ŗ¬Cl¼øŗõĆ»Ź²Ć“ÓĆ£¬Ė÷ŹĻ°±¼ī·Øȱµć£ŗ“óĮæCaCl2ÓĆĶ¾²»“ó£¬NaClĄūÓĆĀŹÖ»ÓŠ70%£¬Ō¼ÓŠ30%µÄNaClĮōŌŚÄøŅŗÖŠ£®
ŗīŹĻÖĘ¼ī·ØµÄÓŵć£ŗ°ŃŗĻ³É°±ŗĶ“æ¼īĮ½ÖÖ²śĘ·ĮŖŗĻÉś²ś£¬ĢįøßĮĖŹ³ŃĪĄūÓĆĀŹ£¬Ėõ¶ĢĮĖÉś²śĮ÷³Ģ£¬¼õÉŁĮĖ¶Ō»·¾³µÄĪŪČ¾£¬½µµĶĮĖ“æ¼īµÄ³É±¾£®±£ĮōĮĖ°±¼ī·ØµÄÓÅµć£¬Ļū³żĮĖĖüµÄȱµć£¬Ź¹Ź³ŃĪµÄĄūÓĆĀŹĢįøßµ½96%£»NH4ClæÉ×öµŖ·Ź£»æÉÓėŗĻ³É°±³§ĮŖŗĻ£¬Ź¹ŗĻ³É°±µÄŌĮĻĘųCO×Ŗ»Æ³ÉCO2£¬¼õÉŁĪŽÓƵÄĀČ»ÆøĘÉś³É£®
½ā“š ½ā£ŗŗīµĀ°ńÖĘ¼īµÄŌĄķ£ŗĻņ°±»ÆµÄ±„ŗĶŹ³ŃĪĖ®ÖŠĶØČė×ćĮ涞Ńõ»ÆĢ¼ĘųĢåĪö³öĢ¼ĖįĒāÄĘ£¬¼ÓČČ·Ö½āĢ¼ĖįĒāÄĘĄ“ÖʱøĢ¼ĖįÄĘ£»·“Ó¦ĪŖ£ŗNaCl+NH3+CO2+H2O=NaHCO3”ż+NH4Cl£¬2NaHCO3$\frac{\underline{\;\;”÷\;\;}}{\;}$Na2CO3+CO2”ü+H2O£¬æɼū¶žŃõ»ÆĢ¼æÉŅŌŃ»·ĄūÓĆ£¬
Ė÷ŹĻ°±¼ī·ØÉś²ś¹ż³ĢÖŠ£¬Éę¼°µÄ·“Ó¦·½³ĢŹ½ÓŠ£ŗNaCl+NH3+CO2+H2OØTNaHCO3”ż+NH4Cl”¢CaCO3ØTCaO+CO2”ü”¢CaO+H2OØTCa£ØOH£©2”¢Ca£ØOH£©2+2NH4ClØTCaCl2+2NH3”ü+2H2O”¢2NaHCO3ØTNa2CO3+H2O+CO2”ü£¬ŹµĻÖĮĖ¶žŃõ»ÆĢ¼ŗĶ°±ĘųµÄŃ»·ĄūÓĆ£¬Č±µć£ŗ“óĮæCaCl2ÓĆĶ¾²»“ó£¬NaClĄūÓĆĀŹÖ»ÓŠ70%£¬Ō¼ÓŠ30%µÄNaClĮōŌŚÄøŅŗÖŠ£¬
ŗīŹĻÖĘ¼ī·ØµÄÓŵć£ŗ°ŃŗĻ³É°±ŗĶ“æ¼īĮ½ÖÖ²śĘ·ĮŖŗĻÉś²ś£¬ĢįøßĮĖŹ³ŃĪĄūÓĆĀŹ£¬Ėõ¶ĢĮĖÉś²śĮ÷³Ģ£¬¼õÉŁĮĖ¶Ō»·¾³µÄĪŪČ¾£¬½µµĶĮĖ“æ¼īµÄ³É±¾£®±£ĮōĮĖ°±¼ī·ØµÄÓÅµć£¬Ļū³żĮĖĖüµÄȱµć£¬Ź¹Ź³ŃĪµÄĄūÓĆĀŹĢįøßµ½96%£¬ĖłŅŌD·ūŗĻ£¬
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éŗīŹĻÖĘ¼ī·ØÓėĖ÷ŹĻ°±¼ī·ØÖŖŹ¶£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņā°ŃĪÕĖ÷¶ūĪ¬ÖĘ¼ī·ØÓėŗīµĀ°ńÖĘ¼ī·Ø·“Ó¦ŌĄķ£¬¼“æÉÅŠ¶Ļ¶žÕßµÄÓÅȱµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ü | B£® | ¢Ł¢Ü¢Ż | C£® | ¢Ł¢Ś¢Ū¢Ü | D£® | ¢Ś¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
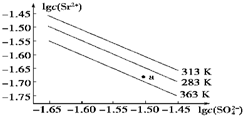
| A£® | ĪĀ¶ČŅ»¶ØŹ±£¬Ksp£ØSrSO4£©Ėęc£ØSO42- £©µÄŌö“ó¶ų¼õŠ” | |
| B£® | Čżøö²»Ķ¬ĪĀ¶ČÖŠ£¬313 KŹ±Ksp£ØSrSO4£©×ī“ó | |
| C£® | 283 KŹ±£¬Ķ¼ÖŠaµć¶ŌÓ¦µÄČÜŅŗŹĒ±„ŗĶČÜŅŗ | |
| D£® | 283 KĻĀµÄSrSO4±„ŗĶČÜŅŗÉżĪĀµ½363 Kŗó±äĪŖ²»±„ŗĶČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬AgClČōŅŖŌŚNaIČÜŅŗÖŠæŖŹ¼×Ŗ»ÆĪŖAgI£¬ŌņNaIµÄÅØ¶Č±ŲŠė²»µĶÓŚ$\frac{1}{\sqrt{1.8}}$”Į10-11 mol•L-1 | |
| B£® | ĻņBaCl2ČÜŅŗÖŠ¼ÓČėAgNO3ŗĶKI£¬µ±Į½ÖÖ³Įµķ¹²“ꏱ£¬$\frac{c£Ø{I}^{-}£©}{c£ØC{l}^{-}£©}$=5.6”Į10-7 | |
| C£® | AgI±ČAgCløüÄŃČÜÓŚĖ®£¬ĖłŅŌ£¬AgClæÉŅŌ×Ŗ»ÆĪŖAgI | |
| D£® | AgCl²»ČÜÓŚĖ®£¬²»ÄÜ×Ŗ»ÆĪŖAgI |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ijĶ¬Ń§Cr2O72-£Øaq£©+H2O£Øl£©?2CrO42-£Øaq£©+2H+£Øaq£©”÷H=+13.8kJ/mol
ijĶ¬Ń§Cr2O72-£Øaq£©+H2O£Øl£©?2CrO42-£Øaq£©+2H+£Øaq£©”÷H=+13.8kJ/mol| A£® | øĆ·“Ó¦ŹĒŅ»øöŃõ»Æ»¹Ō·“Ó¦ | |
| B£® | “żŹŌ¹ÜbÖŠČÜŅŗŃÕÉ«²»±äµÄÄæµÄŹĒŹ¹Cr2O72-ĶźČ«·“Ó¦ | |
| C£® | øĆŹµŃé²»ÄÜÖ¤Ć÷¼õŠ”Éś³ÉĪļÅØ¶Č£¬Ę½ŗāÕżĻņŅĘ¶Æ | |
| D£® | ŹŌ¹ÜcÖŠµÄĻÖĻóĖµĆ÷Ó°ĻģĘ½ŗāµÄÖ÷ŅŖŅņĖŲŹĒĪĀ¶Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

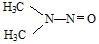 ĖłŹ¾£¬1molNDMA·Ö×ÓÖŠŗ¬ÓŠ¦Ņ¼üµÄŹżÄæĪŖ10mol£®
ĖłŹ¾£¬1molNDMA·Ö×ÓÖŠŗ¬ÓŠ¦Ņ¼üµÄŹżÄæĪŖ10mol£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪĀ¶Č | 250”ę | 300”ę | 350”ę |
| K | 2.041 | 0.270 | 0.012 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com