
| A、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH |
| B、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| C、向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+=SO2↑+H2O |
| D、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3?H2O+H2O |


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
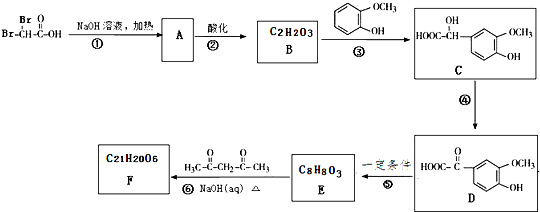
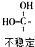
| 转化 |
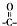 +H2O
+H2O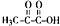
| 一定条件 |
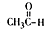 +CO2
+CO2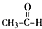 +
+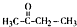
| NaOH(aq) |
| △ |
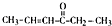 +H2O
+H2O查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯与溴水混合振荡,水层颜色变浅 |
| B、裂化汽油与溴水混合振荡,水层颜色变浅 |
| C、乙烯与水在一定条件下反应制取乙醇 |
| D、乙炔与氯化氢在一定条件下反应制取氯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤燃烧是化学能转化为光能的过程 |
| B、1 mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
| C、HCl 和 NaOH 反应的中和热△H=-57.3 kJ/mol,则H2SO4和 Ca(OH)2 反应的中和热△H=2×(-57.3)kJ?mol-1 |
| D、反应 H2(g)+F2(g)═2HF(g);△H=-270 kJ?mol-1说明在相同条件下,1 mol 氢气与 1 mol 氟气的能量总和大于2 mol 氟化氢气体的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO2 |
| B、NO |
| C、N2O |
| D、NH4NO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com