

| A、图①两极均有气泡产生,滴加酚酞溶液时石墨一极变红 |
| B、图②装置可以验证牺牲阳极的阴极保护法 |
| C、图③可以模拟钢铁的吸氧腐蚀,碳棒一极的电极反应式:O2+2H2O+4e-=4OH- |
| D、分别给上述4个装置的铁电极附近滴加少量K3[Fe(CN)6]溶液,②④出现蓝色沉淀 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
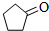 )可由环戊烷经三步反应合成:
)可由环戊烷经三步反应合成: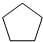
| 反应1 |
| 反应2 |
| 反应3 |
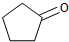
| A、反应1可用试剂是氯气 |
| B、反应3可用的试剂是氧气和铜 |
| C、反应1为取代反应,反应2为消去反应 |
| D、A可通过加成反应合成Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
 -定条件下,在绝热恒容2L密闭容器中进行反应N2(g)+3H2(g)?2NH3(g)△H<0,若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中一定正确的是( )
-定条件下,在绝热恒容2L密闭容器中进行反应N2(g)+3H2(g)?2NH3(g)△H<0,若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中一定正确的是( )| A、若在t2时刻再充入一定量He,达平衡时c(H2)<0.4mol/L |
| B、a点表示NH3生成速率与NH3分解速率相等 |
| C、b点和c点H2的转化率相等 |
| D、若在t2时刻再充入一定量He,达平衡时化学平衡常数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用二氧化碳制造全降解塑料,可以减缓二氧化碳对环境的影响 |
| B、淀粉、油脂、蛋白质都能在人体内水解,也能在体内氧化提供能量 |
| C、CO2与SiO2都是ⅣA族元素的氧化物,但它们的物理性质特别是在熔沸点、硬度上相差很大,这是由于它们的化学键类型不同造成的 |
| D、酸碱质子理论认为,凡能给出质子(H+)的物质都是酸,凡能接受质子的物质都是碱.根据这一理论,Al(OH)3、NaHCO3都是酸碱两性物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式为2CH4O+3O2=2CO2+4H2O,如图是该燃料电池的示意图.下列说法错误的是( )
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式为2CH4O+3O2=2CO2+4H2O,如图是该燃料电池的示意图.下列说法错误的是( )| A、a是甲醇,b是氧气 |
| B、燃料电池将化学能转化为电能 |
| C、质子从M电极区穿过交换膜移向N电极区 |
| D、负极反应:CH4O-6e-+H2O=CO2↑+6H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、沸点:NH3>PH3>AsH3 |
| B、结合质子的能力:OH->CH3COO->Cl- |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Fe3+、NO3-、Cl2都可在该物质的溶液中大量共存 |
B、 向O.1mo1-L-1该物质的溶液中清加0.Lmol-1NaOH溶液,生成沉淀的物质的量与逐滴加入NaOH溶液体积关系如图所示 |
| C、检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色 |
| D、向该物质的溶液中摘加Ba(OH)2溶液,恰好使S042-完全沉淀的离子方程式为:Fe2++2SO42-+3Ba2++2OH-═2BaSO4↓+Fe(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用足量的KMnO4溶液吸收SO2气体:2MnO4+5SO2+2H2O=2Mn2-+5SO42-+4H+ | ||||
| B、Ca(ClO)2溶液与Na2SO3溶液混合:Ca2++SO32-=CaSO3↓ | ||||
C、NH4HSO3溶液与足量NaOH溶液共热:NH4++2OH-
| ||||
D、已知H2的燃烧热△H=-285.8kj?mol-1,则用热化学方程式可表示为:H2(g)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol NH3 |
| B、标准状况下22.4 L He |
| C、4℃时 9 mL 水 |
| D、0.2 mol H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com