
【题目】下列反应属于加成反应的是
A.乙酸与NaOH溶液反应B.乙烯使酸性KMnO4溶液褪色
C.甲烷气体燃烧D.乙烯与水反应制乙醇
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.汽油、煤油、柴油均可来自于石油的分馏
B.煤的液化与气化都是物理变化
C.乙烯和苯均能使酸性高锰酸钾溶液褪色
D.乙炔和苯均能使溴水褪色且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K、1.01×105Pa,O2、S、Se、Te分别与H2化合的反应热数据如图所示。写出Se与H2化合的热化学反应方程式正确的是

A. Se(s)+ H2(g) = H2Se(g) ΔH=-242kJ·mol-1
B. Se(s)+ H2(g) = H2Se(g) ΔH=-20kJ·mol-1
C. Se(g)+ H2(g) = H2Se(g) ΔH=+81kJ·mol-1
D. Se(s)+ H2(g) = H2Se(g) ΔH=+81kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I5表示)如表所示:
I1 | I2 | I3 | I4 | I5 | |
电离能 | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是_________价,其基态原子电子排布式为_________。
(2)Ca3(PO4)3F中非金属元素电负性由大到小的顺序为_________。
(3)PO43-的中心原子的杂化方式为_________,该离子的空间构型为_________,键角为________,其等电子体有_________ (请写出两种)。
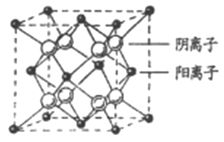
(4)CaF2晶胞结构如图所示,则CaF2晶体中与Ca2+最近且等距离的Ca2+数目为_________;已知Ca2+和F半径分别为a cm、b cm,阿伏加德罗常数为NA,M为摩尔质量,则晶体密度为________g·cm3(不必化简)。
(5)已知MgO与CaO的晶体结构相似,其摩氏硬度的大小关系为_________,原因为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置(气密性良好),若先将甲中液体滴入丙中,观察到气球明显鼓起,一段时间后恢复原状;再将乙中液体滴入丁中,气球又明显鼓起。下列组合正确的是( )

选项 | 滴管甲 | 烧杯丙 | 滴管乙 | 烧杯丁 |
A | 双氧水 | 二氧化锰 | 水 | 氢氧化钙 |
B | 稀硫酸 | 镁 | 盐酸 | 碳酸钙 |
C | 水 | 氢氧化钠 | 水 | 硝酸铵 |
D | 水 | 氧化钙 | 盐酸 | 镁 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有以下物质:①熔化的NaOH ②稀H2SO4溶液 ③KNO3 固体 ④汞(金属)⑤酒精(C2H5OH)溶液 ⑥干冰,请回答下列问题(用序号填空):
①属于电解质的是______________________;
②属于非电解质的是___________________。
(2)有四种物质是:①标况下6.72L CH4;②3.01×1023个HCl;③13.6g H2S;④0.2mol NH3,其中含有原子数最多的是_________,质量最大的是________。(用序号填空)
(3)如图所示,隔板I、Ⅱ均可自由移动,保持温度相同,若M容器中充入O2,N容器中充入SO2,若两容器中所含气体质量相等,则M容器和N容器的体积比为___________;若M容器中充入CO2,N容器中充入CO和H2两种混合气体,若隔板不再移动时两容器体积比为1:1, 则M,N容器中原子总数比为___________。
(4)标况下,体积_____L的CO气体含电子数与1.7克氢氧根离子OH- 含的电子数相同。
(5)9.5 g MCl2中含有Cl-的物质的量为0.2mol,则该氯化物的摩尔质量为________ g/mol,其中含M2+ 的质量为______g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】aL体积比为1∶3的A、B两种链烃的混合气体,可与0.5aL(状态相同)氢气发生加成反应,则A、B两种链烃的通式可能是( )
A. CnH2n-2和CnH2n+2B. C nH2n和CnH2n+2
C. CnH2n和CnH2nD. CnH2n和CnH2n-2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为将含有的FeCl3、FeCl2、CuCl2的废液中的Cu2+还原回收,某同学在含有ag铁粉的容器中加入废液,探究了加入废液体积与完全反应后体系中固体质量的关系,部分实验数据如下表所示。已知:废液中c(Cu2+)=0.7 mol·Lˉ1;废液体积大于0.5L,充分反应后才能检测出Cu2+。

下列说法不正确的是
A. 当铁粉与0.25L废液反应完全后,固体成分为Fe与Cu
B. 当铁粉与1L废液反应完全后,再加入废液时发生的离子反应为Fe +2Fe3+=3Fe2+
C. 废液中c(Fe3+)=0.2 mol·Lˉ1
D. 要将1L废液中的Cu2+全部还原,则至少需要铁粉44.8g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com