
| A. | 验证淀粉水解产物时,在淀粉溶液中加几滴稀硫酸,水浴5min,加入新制银氨溶液 | |
| B. | 煤油可由石油分馏获得,可用作燃料和保存少量的金属钠 | |
| C. | 向2mLl0%NaOH溶液中滴入2%CuS04溶液的4-6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾,则有砖红色沉淀出现 | |
| D. | 植物油能使溴的四氯化碳溶液褪色,盛过油脂的试管用碱液洗涤 |
分析 A.淀粉水解后显酸性,检验葡萄糖应在碱性条件下;
B.根据煤油和钠的性质判断;
C.醛的氧化性实验需在碱性环境下进行,2%CuS04溶液的4-6滴,碱足量;
D.植物油高级脂肪烃基含有C=C官能团,盛过油脂的试管可用热碱溶液进行洗涤.
解答 解:A.淀粉水解后显酸性,检验葡萄糖应在碱性条件下,则验证淀粉水解产物时,在淀粉溶液中加几滴稀硫酸,然后加碱呈碱性,水浴5min,再加入新制银氨溶液检验水解产物,故A错误;
B.石油分馏可得到煤油,煤油是碳氢化合物能燃烧,煤油和钠不反应,且钠的密度大于煤油的密度,所以煤油能保存少量金属钠,故B正确;
C.葡萄糖与新制氢氧化铜反应应在碱性环境中反应,向2mLl0%NaOH溶液中滴入2%CuS04溶液的4-6滴,碱足量,振荡后加入乙醛溶液0.5mL,加热至沸腾,则有砖红色沉淀出现,故C正确;
D.植物油高级脂肪烃基含有C=C官能团,能与溴发生加成反应而使溴的四氯化碳溶液褪色,油脂在碱性条件下发生水解,所以常能用热的碱液来洗涤沾有油脂的试管,故D正确;
故选A.
点评 本题考查了淀粉水解产物的检验、煤油的性质、葡萄糖的检验以及油脂的性质,注意醛基的检验需在碱性环境中反应是解题的关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
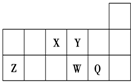
| A. | 元素X与元素Z的最高正化合价之和的数值等于8 | |
| B. | 原子半径的大小顺序为:Y>Z | |
| C. | 离子Y2-和Z3+的核外电子总数和电子层数都不相同 | |
| D. | 元素W的单质比Q的熔点低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实 验 操 作 | 现 象 | 实 验 结 论 | |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有SO42- |
| B | 将某气体通入澄清石灰水中 | 变浑浊 | 该气体一定是CO2 |
| C | 向某溶液中加入2滴KSCN溶液; | 溶液不显红色; | 溶液中一定含有Fe2+ |
| 另取样,先滴入氯水,再滴入KSCN溶液 | 溶液变为红色 | ||
| D | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ⑤⑥⑦ | C. | ①②⑦ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
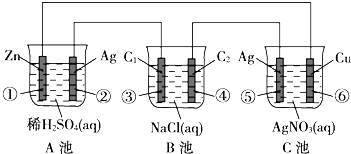 已知金属活动性相差越大,形成原电池时越容易放电.请根据如图装置,回答下列问题:(其中C1、C2都为石墨电极)
已知金属活动性相差越大,形成原电池时越容易放电.请根据如图装置,回答下列问题:(其中C1、C2都为石墨电极)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑥⑦ | B. | ②④⑤ | C. | ①③⑥ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图①表示可逆反应CO(g)+H2O(g)?CO2(g)+H2(g)中的△H大于0 | |
| B. | 图②是石墨为电极电解氯化钠稀溶液,阴、阳两极产生气体体积之比一定为1:1 | |
| C. | 图③表示25℃,0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,pH随加入酸体积的变化 | |
| D. | 图④表示2SO2(g)+O2(g)?2SO3(g)△H<0 正、逆反应平衡常数K随温度的变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com