
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年河北定州中学高一承智班12月月考化学卷(解析版) 题型:选择题
已知Q与R的摩尔质量之比为9:22,在反应X+2Y===2Q+R中,当1.6g X与Y完全反应后,生成4.4g R,则参与反应的Y和生成物Q的质量之比为( )
A.46∶9 B.32∶9 C.23∶9 D.16∶9
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上期中化学卷(解析版) 题型:选择题
下列溶液中有关的化学方程式,正确的是( )
A.NaHCO3的电离方程式:NaHCO3=Na++H++CO32-
B.Na投入硫酸铜溶液反应的化学方程式:2Na+CuSO4=Cu+Na2SO4
C.Ca(HCO3)2与澄清石灰水反应的离子方程式:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.Ba(OH)2的电离方程式:Ba(OH)2=Ba2++(OH)2-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上期中化学卷(解析版) 题型:选择题
根据下列实验事实得出的相应结论正确的是( )
序号 | 实验事实 | 结论 |
A | 气体A的水溶液可以导电 | A不一定是电解质 |
B | 向某溶液中加入BaCl2溶液和稀HNO3,有白色沉淀生成 | 原溶液中含SO42- |
C | 向某溶液中滴加CCl4,振荡、静置,下层溶液呈紫红色 | 原溶液中一定有I- |
D | 某钠盐加入盐酸,若有气体生成 | 该盐一定是碳酸钠 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一12月月考化学卷(解析版) 题型:推断题
A、B、C、D、 E五种化合物中均含有地壳中含量最多的金属元素,它们的转化关系如图所示,其中A为澄清溶液,B、C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
E五种化合物中均含有地壳中含量最多的金属元素,它们的转化关系如图所示,其中A为澄清溶液,B、C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
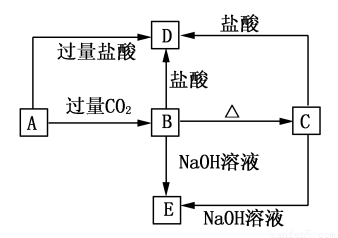
(1)写出化学式:A________,B________,C________,D________,E________。
(2)写出下列反应的离子方程式:
A→B:_____________________
A→D:_____________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一12月月考化学卷(解析版) 题型:选择题
在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中加入足量的Na2O2固体,充分作用后,再加入过量的稀盐酸,完全反应,则离子数目没有变化的是( )
A.Fe3+、Al3+ B.Al3+
C.Fe2+、NH4+ D.Fe3+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二12月月考化学卷(解析版) 题型:选择题
利用右图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是 ( )
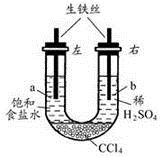
A. a管发生吸氧腐蚀,b管发生析氢腐蚀
B. 一段时间后,a管液面高于b管液面
C. a处溶液的pH增大,b处溶液的pH减小
D. a、b两处具有相同的电极反应式:Fe-2e-=Fe2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南浏阳一中等两校高二12月联考化学卷(解析版) 题型:填空题
部分弱酸的电离平衡常数如表。
弱酸 | HCOOH | H2S | H2SO3 |
电离平衡常数 (25℃) | K=1.8×10-4 | K1=9.1×10-8 K2=1.1×10-12 | K1=1.23×1 K2=6.6×10-8 |
(1)物质的量均为0.1mol/L的溶液①HCO ONa②NaHS③Na2SO3,pH最大的是________(填编号)
ONa②NaHS③Na2SO3,pH最大的是________(填编号)
(2)设计实验证明HCOOH为弱酸
(3)室温下,下列溶液中水电离出的c(H+)水由大到小的顺序为________(填编号)
①pH=12的NaOH溶液 ②NaCl溶液 ③pH=6的NH4Cl溶液 ④0.01mol/L醋酸
(4)二元酸H2A在水中存在以下电离:H2A=H++HA-,HA- H++A2-,试回答下列问题:
H++A2-,试回答下列问题:
①NaHA溶液呈 (填“酸性”、“碱性”、“中性” )
②某温度下,10mL、0.1mol/LNaHA溶液中加入0.1mol/LKOH溶液VmL至中性,此时溶液中以下关系一定正确的是(  )
)
A.溶液的pH=7 B.Kw=c2(OH-) C.V=10 D.c(K+)< c(Na+)
(5)如图横坐标为室温下溶液的pH,纵坐标为金属离子物质的量浓度的对数(当溶液中金属离子浓度≤10-5mol/L时,可认为沉淀完全)。试回答:
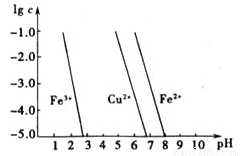
腐蚀铜板的溶液中,若Cu2+、Fe3+、Fe2+浓度均为0.1mol/L,向混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为 。
从图中的数据计算可得Fe(OH)2溶度积Ksp[Fe(OH)2]= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com