



 +2NaOH
+2NaOH
 +HCOONa+H2O
+HCOONa+H2O +2NaOH
+2NaOH
 +HCOONa+H2O
+HCOONa+H2O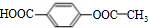 ,故B结构简式为
,故B结构简式为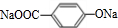 ,B溶液中通入气体C生成D,D不能与NaHC03溶液反应,但能与NaOH溶液反应,则D中有酚羟基并无羧基,则说明酸化的物质其酸性介于酚与羧酸之间,气体C应是二氧化碳,故D为
,B溶液中通入气体C生成D,D不能与NaHC03溶液反应,但能与NaOH溶液反应,则D中有酚羟基并无羧基,则说明酸化的物质其酸性介于酚与羧酸之间,气体C应是二氧化碳,故D为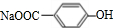 ,D酸化得到F,F为
,D酸化得到F,F为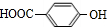 ,D与浓溴水反应生成G,G为
,D与浓溴水反应生成G,G为 ,乙酸钠酸化得到E,E为乙酸,据此解答.
,乙酸钠酸化得到E,E为乙酸,据此解答. ,故B结构简式为
,故B结构简式为 ,B溶液中通入气体C生成D,D不能与NaHC03溶液反应,但能与NaOH溶液反应,则D中有酚羟基并无羧基,则说明酸化的物质其酸性介于酚与羧酸之间,气体C应是二氧化碳,故D为
,B溶液中通入气体C生成D,D不能与NaHC03溶液反应,但能与NaOH溶液反应,则D中有酚羟基并无羧基,则说明酸化的物质其酸性介于酚与羧酸之间,气体C应是二氧化碳,故D为 ,D酸化得到F,F为
,D酸化得到F,F为 ,D与浓溴水反应生成G,G为
,D与浓溴水反应生成G,G为 ,乙酸钠酸化得到E,E为乙酸,
,乙酸钠酸化得到E,E为乙酸, ,含有羧基、酚羟基;
,含有羧基、酚羟基; 在酸性条件下水解的产物为
在酸性条件下水解的产物为 、CH3COOH,二者都可以发生取代反应,
、CH3COOH,二者都可以发生取代反应, 含有苯环,可以发生加成反应,含有羧基、羟基,可以发生缩聚反应,不能发生消去反应与加聚反应,
含有苯环,可以发生加成反应,含有羧基、羟基,可以发生缩聚反应,不能发生消去反应与加聚反应,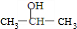 等,名称为2-丙醇,
等,名称为2-丙醇, ,
, :
: 的同分异构体,苯环上两个取代基在对位;M与A具有相同的官能团,但与新制氢氧化铜悬浊液共热有砖红色沉淀生成,M为
的同分异构体,苯环上两个取代基在对位;M与A具有相同的官能团,但与新制氢氧化铜悬浊液共热有砖红色沉淀生成,M为 等,与NaOH溶液反应的化学方程式为
等,与NaOH溶液反应的化学方程式为 +2NaOH
+2NaOH
 +HCOONa+H2O,
+HCOONa+H2O, +2NaOH
+2NaOH
 +HCOONa+H2O.
+HCOONa+H2O.

科目:高中化学 来源: 题型:
 (2012?焦作一模)某同学在三个容积相同的密闭容器中,研究三种不同条件下化学反应2X(g)?Y(g)+W(g)的进行情况,其中实验Ⅰ、Ⅱ控温在T1,实验Ⅲ控温在T2,它们的起始浓度均是c(X)=1.0mol?L-1,c(Y)=c(W)=0,测得反应物X的浓度随时间的变化如图所示,下列说法不正确的是( )
(2012?焦作一模)某同学在三个容积相同的密闭容器中,研究三种不同条件下化学反应2X(g)?Y(g)+W(g)的进行情况,其中实验Ⅰ、Ⅱ控温在T1,实验Ⅲ控温在T2,它们的起始浓度均是c(X)=1.0mol?L-1,c(Y)=c(W)=0,测得反应物X的浓度随时间的变化如图所示,下列说法不正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
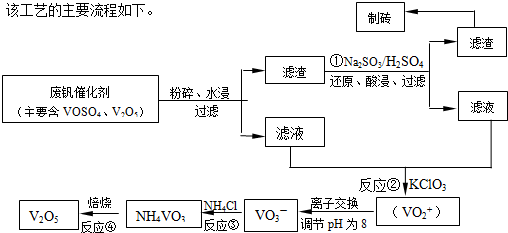
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
| ||
| ||
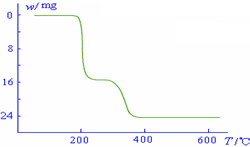 化的曲线如右图所示.则NH4VO3在分解过程中
化的曲线如右图所示.则NH4VO3在分解过程中查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com