
| A. | 高铁酸钠中铁显+6价 | |
| B. | 湿法中每生成1 mol Na2FeO4转移3 mol电子 | |
| C. | 干法中每生成1 mol Na2FeO4转移3 mol电子 | |
| D. | Na2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质 |
分析 K2FeO4处理水时,与水不发生氧化还原反应,具有强氧化性,且还原产物铁离子水解生成胶体可净化水,并利用化合价的变化计算转移电子,以此来解答.
解答 解:A.根据化合价代数和为0的原则可知,高铁酸钾中铁显+6价,故A正确;
B.湿法中每生成1molNa2FeO4,有1molFe(OH)3参加反应,化合价由+3价升高到+6价,转移电子3mol,故B正确;
C.干法中每生成1molNa2FeO4,有1molFeSO4参加反应,化合价由+2价升高到+6价,且O元素化合价由-1价变化为0价,则转移电子5mol,故C错误;
D.K2FeO4具有强氧化性,发生氧化还原反应能除去H2S、NH3等,可用于消毒杀菌,被还原为Fe3+,水解生成Fe(OH)3,具有吸附性,可用于吸附水中的悬浮杂质,故D正确.
故选C.
点评 本题考查氧化还原反应,为高频考点,注意不同制备方法的反应原理,把握元素化合价的判断方法,从化合价变化的角度分析氧化还原反应,侧重分析与迁移应用能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 金属单质在常温下都是固体 | |
| B. | 金属原子只有还原性,金属阳离子只有氧化性 | |
| C. | 含金属元素的离子都是阳离子 | |
| D. | 金属阳离子被还原不一定生成金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
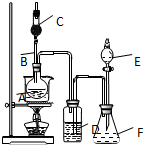 为证明乙醇分子中含有氧原子,运用R-OH+HCl═RCl+H2O反应生成的水(H2O),检测其中的氧.现采用一套如图所示装置进行实验. 装置中所装的试剂:
为证明乙醇分子中含有氧原子,运用R-OH+HCl═RCl+H2O反应生成的水(H2O),检测其中的氧.现采用一套如图所示装置进行实验. 装置中所装的试剂:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
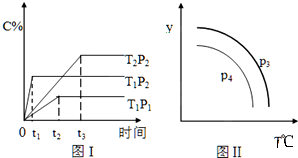
| A. | x=2,T1>T2,P2>P1 | |
| B. | P3>P4,y轴表示B的质量分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3>P4,y轴表示混合气体的平均摩尔质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 近年来流行喝苹果醋.苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸(α-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )
近年来流行喝苹果醋.苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸(α-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )| A. | 苹果酸在一定条件下能发生酯化反应 | |
| B. | 苹果酸在一定条件下能发生催化氧化反应 | |
| C. | 苹果酸在一定条件下能发生消去反应 | |
| D. | 1 mol苹果酸与Na反应必须消耗2 mol Na |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
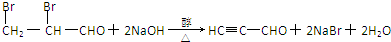 .
.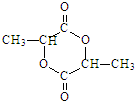 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
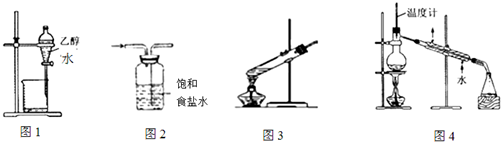
| A. | 图1装置用于分离乙醇和水 | B. | 图2装置用于除去氯气中的氯化氢 | ||
| C. | 图3装置用于葡萄糖的银镜反应 | D. | 图4装置用于石油的蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
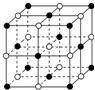 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知: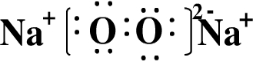 ,含有的化学键类型为离子键和共价键,Z2Y2为离子晶体.
,含有的化学键类型为离子键和共价键,Z2Y2为离子晶体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com