
分析 (1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体,反应的方程式为2As2S3+2SnCl2+4HCl=As4S4+2SnCl4+2H2S↑,可根据方程式或化合价的变化判断;
(2)反应中As和Sn元素化合价发生变化,根据化合价的变化判断氧化剂和还原剂等概念;
(3)根据化合价的升降以及物质的量的情况来计算转移电子的量;NO3-发生还原反应生成二氧化氮,所以二氧化氮在正极附近逸出;
(4)根据化合价的变化计算电子转移的数目,进而结合反应的关系式可确定生成二氧化碳的物质的量.
解答 解:(1)根据电子得失守恒知1molAs2S3作氧化剂得到2mol电子,而1molSnCl2作还原剂失去2mol电子,所以二者的物质的量之比是1:1,故答案为:1:1;
(2)反应中As元素化合价降低,As2S3为氧化剂,H2S为酸性气体,可用NaOH溶液吸收,故答案为:As2S3;NaOH溶液;
(3)反应As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O中,As元素化合价由+3价升高到+5价,S元素化合价由-2价升高到0价,则生成2mol H3AsO4,转移电子为2×2mol+3×2mol=10mol,NO3-发生还原反应生成二氧化氮,所以二氧化氮在正极附近逸出,故答案为:10mol;正极;
(4)反应的关系式为O2~4HNO3~CO2,
n(O2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,根据电子守恒可知生成CO2的量是0.5mol,但考虑到随着反应到进行,硝酸的浓度会降低而稀硝酸不与碳反应,则生成的二氧化碳的物质的量少于0.5mol,
故答案为:a.
点评 本题综合考查氧化还原反应的计算和概念的理解,为高考常见题型,侧重于学生的分析能力和计算能力的考查,有利于培养学生的化学科学素养,难度不大,注意从元素化合价的角度识别相关概念、判断物质的性质.


科目:高中化学 来源: 题型:计算题
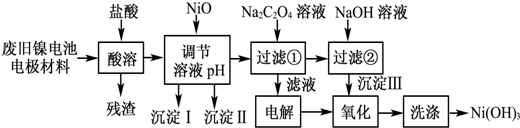
| M(OH)n | Ksp | 开始沉淀pH | 沉淀完全pH |
| Al(OH)3 | 1.9×10-23 | 3.4 | 4.2 |
| Fe(OH)3 | 3.8×10-38 | 2.5 | 2.9 |
| Ni(OH)2 | 1.6×10-14 | 7.6 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x=1 | |
| B. | A的平均反应速率为0.3mol/(L•s) | |
| C. | B的转化率为60% | |
| D. | 若混合气体的密度不再改变时,该反应一定达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
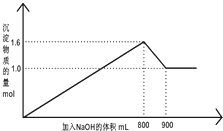 向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:
向1L A1Cl3和FeCl3的混合溶液,逐滴加入NaOH 的溶液.产生沉淀的物质的量和加入溶液的体积的关系如图所示,回答下列问题:| 溶质 | A1Cl3 | FeCl3 |
| 物质的量浓度 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ①③ | D. | ①②③全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②④⑤ | C. | ①②③④⑤ | D. | 只有⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C4H6 | B. | C3H6 | C. | C3H8 | D. | C5H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2和H4SiO4 | B. | O2和SiO2 | C. | CO2和Na2CO3 | D. | H2和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑥ | B. | ③⑤⑥ | C. | ②④⑦ | D. | ③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com